chemica@paran.com
| FID를 이용한 HC 농도 측정 (1) 화염이온화 감지법(FID ;Flame Ionization Detection) 이란 탄화수소 농도는 일반적으로 불꽃 이온화 감지기(FID; Flame Ionization Detector)를 사용하여 측정한다. 미연탄화수소가 포함된 샘플가스는 수소 또는 수소-헬륨 불꽃에서 연소되고, 이온은 화학적 이온화 과정에서 소비되는 샘플가스 중 탄소에 의해서만 생성되므로 샘플가스가 유입되지 않은 상태에서는 생성되지 않는다. 이온전류의 크기는 미연탄화수소 농도 또는 미연탄화수소 중 탄소 원자의 개수를 통한 양적 측정을 제공한다. 빠른 응답의 FID 기구는 자동차 응용 여러 분야에서 탄화 수소 측정에 넓게 사용되고 있다. |
출처: <http://ws.ajou.ac.kr/~tperc/research_3.htm>
FID(Flame Lonization Detector) : 불꽃이온화 검출기
원리는 수소/Air에 의해 형성된 불꽃에서 시료가 연소되면 전하를 띤 이온이 형성되며, 이온의 농도에 비례하여 전류 흐름이 변화 된다. 구조는 jet(컬럼의 종류에 따라 사용되는 Jet의 크기가 구분), 수소 및 Air inlet, FID collector Assembly로 나뉜다. 주요 특징으로는 Sensitivity(대부분의 화합물에 대해 TCD의 약 103배 정도 감도가 높다.), Selectivity(수소/Air에 의한 불꽃에서 태워져 전하를 띤 이온을 생성하는 화합물만 검출할 수 있는 선택적인 검출기)이다.
FID에서 검출되지 않는 성분들 : Rare Gas (수소, 아르곤), 질소, 이산화질소, 일산화탄소, 이산화탄소, 사염화탄소, 이산화황, 산소, 물……등
주입구의 역할: 시료성분을 충분히 기화시키는데 최적인 온도 설정이 필요하므로 이를 맞춰 주어야 함.
(설정온도가 너무 높았을 경우 시료에 따라서는 분해를 일으키는 일도 있고 낮은 경우는 피크가 브로드하게 되는 일도 있기 때문에 주의가 필요)
1. 스프리트/스프리트레스 주입구
스프리트 주입구는 시료 부하용량이 작은 캐필러리 컬럼에 시료를 도입하기 위해서 고안, 시료주입구에서 도입되고 기화한 시료의 일부만을 분리컬럼에 이끌고 그 이외는 계외에 배출하는 장치로 피크를 샤프하게 하는 효과가 있다.
하지만 저농도의 시료분서에는 좋지 않다. 또 비점의 범위가 넓은 시료에서는 스프리트비가 일정하지 않는 경우도 있기 때문에 주의가 필요하다.
또 시료 도입시만 스프리트 가스를 멈추어 기화한 시료의 대부분을 캐필러리 컬럼에 도입하는 것이 스프리트레스 주입법이다. 용매의 큰 피크의 뒤에 테일링피크 부분을 없애는 것이나 컬럼항온조의 온도를 용매의 비점보다 낮게 억제하는 것으로 컬럼의 선단에 분석종을 농축하는 방법을 이용하는 것이 가능하여 저농도의 시료분석에도 대응 가능하다.
다만 스프리트 주입구와 스프리트레스 주입구의 어느 쪽이나 시료를 실린지로 도입해 기화시킬 단계에서 디스크리미네이션을 일으키는 일이 있어 성분의 비율이 바뀌어 버리는 일이 있기 때문에 주의가 필요하다.
스프리트 주입구는 스프리트레스 주입구를 겸하고 있는 경우도 많고 그 경우를 스프리트/스프리트레스 주입구라 부른다.
출처: <http://01041902024.tistory.com/149>
Flame ionization detector
From Wikipedia, the free encyclopedia
Jump to: navigation, search
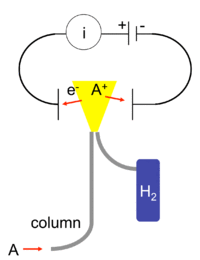
Schematic of a flame ionization detector for gas chromatography
A flame ionization detector (FID) is a scientific instrument that measures the concentration of organic species in a gas stream. It is frequently used as a detector in gas chromatography. Standalone FIDs can also be used in applications such as landfill gas monitoring, fugitive emissions monitoring and internal combustion engine emissions measurement[1] in stationary or portable instruments.
Contents
[hide]
- 1 History
- 2 Operating principle
- 3 Advantages and disadvantages
- 4 Operation
- 5 Description of a generic detector
- 6 See also
- 7 References
- 8 Sources
History[edit]
The first flame ionization detectors were developed simultaneously and independently in 1957 by scientists working for the Commonwealth Scientific and Industrial Research Organisation (CSIRO) in Melbourne, Australia.[2][3][4] and at the University of Pretoria in Pretoria, South Africa.[5]
In 1959, Perkin Elmer Corp. included a flame ionization detector in its Vapor Fractometer[6]
Operating principle[edit]
The operation of the FID is based on the detection of ions formed during combustion of organic compounds in a hydrogen flame. The generation of these ions is proportional to the concentration of organic species in the sample gas stream. Hydrocarbons generally have molar response factors that are equal to number of carbon atoms in their molecule, while oxygenates and other species that contain heteroatoms tend to have a lower response factor. Carbon monoxide and carbon dioxide are not detectable by FID.
Advantages and disadvantages[edit]
Advantages[edit]
Flame ionization detectors are used very widely in gas chromatography because of a number of advantages.
- Cost: Flame ionization detectors are relatively inexpensive to acquire and operate.
- Low maintenance requirements: Apart from cleaning or replacing the FID jet, these detectors require no maintenance.
- Rugged construction: FIDs are relatively resistant to misuse.
- Linearity and detection ranges: FIDs can measure organic substance concentration at very low and very high levels, having a linear response of 10^6.
Disadvantages[edit]
Flame ionization detectors cannot detect inorganic substances. In some systems, CO and CO2 can be detected in the FID using a methanizer, which is a bed of Ni catalyst that reduces CO and CO2 to methane, which can be in turn detected by the FID.
Another important disadvantage is that the FID flame oxidizes all compounds that pass through it; all hydrocarbons and oxygenates are oxidized to carbon dioxide and water and other heteroatoms are oxidized according to thermodynamics. For this reason, FIDs tend to be the last in a detector train and also cannot be used for preparatory work.
Operation[edit]
In order to detect these ions, two electrodes are used to provide a potential difference. The positive electrode doubles as the nozzle head where the flame is produced. The other, negative electrode is positioned above the flame. When first designed, the negative electrode was either tear-drop shaped or angular piece of platinum. Today, the design has been modified into a tubular electrode, commonly referred to as a collector plate. The ions thus are attracted to the collector plate and upon hitting the plate, induce a current. This current is measured with a high-impedance picoammeter and fed into an integrator. The manner in which the final data is displayed is based on the computer and software. In general, a graph is displayed that has time on the x-axis and total ion on the y-axis.
The current measured corresponds roughly to the proportion of reduced carbon atoms in the flame. Specifically how the ions are produced is not necessarily understood, but the response of the detector is determined by the number of carbon atoms (ions) hitting the detector per unit time. This makes the detector sensitive to the mass rather than the concentration, which is useful because the response of the detector is not greatly affected by changes in the carrier gas flow rate.
Description of a generic detector[edit]
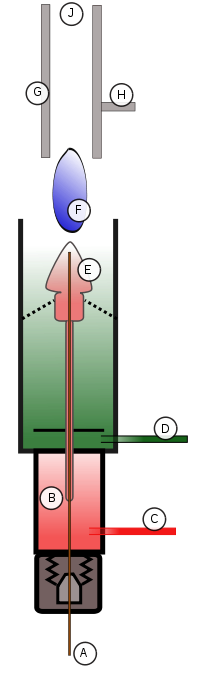
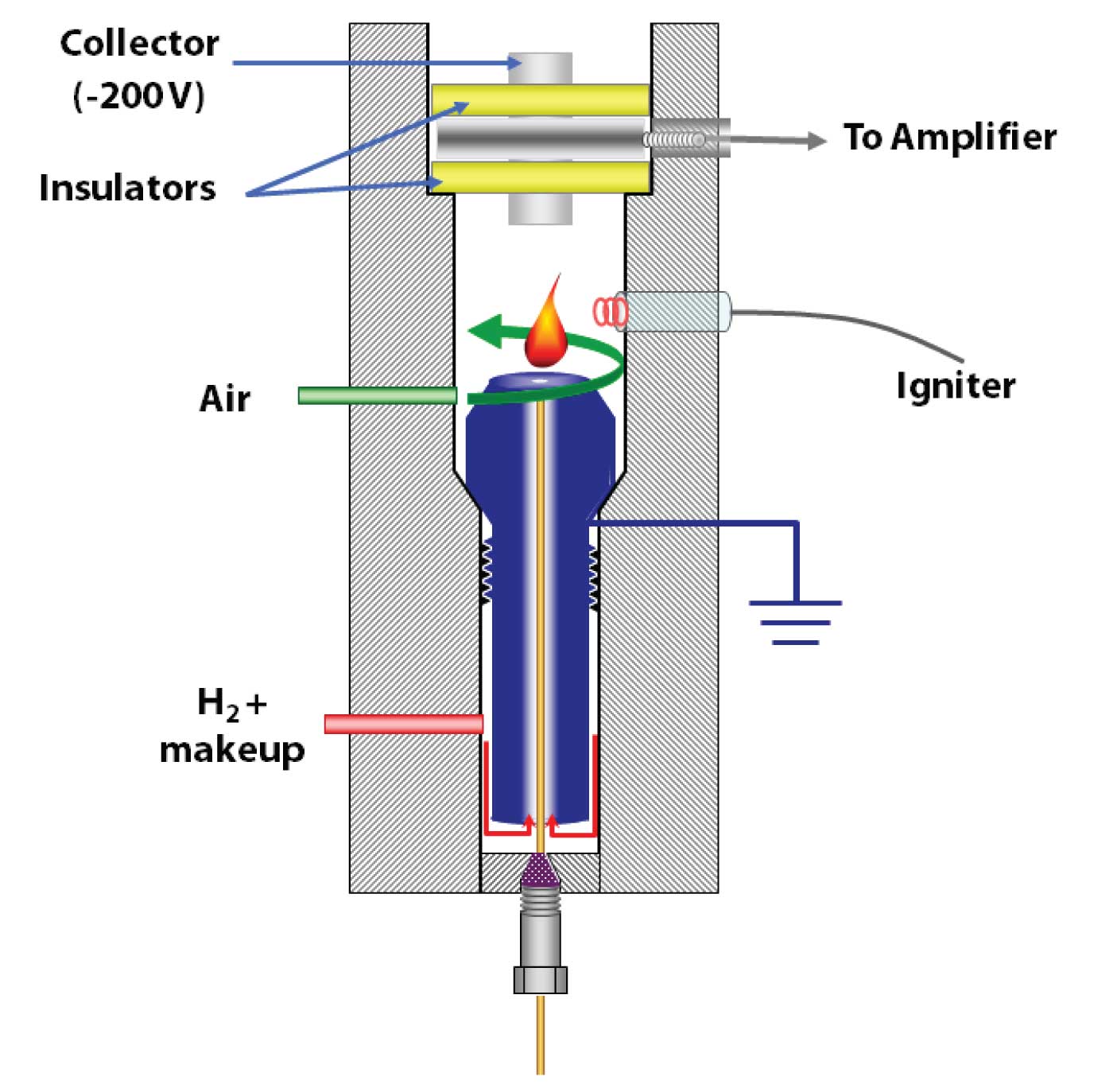
FID Schematic
The design of the flame ionization detector varies from manufacturer to manufacturer, but the principles are the same. Most commonly, the FID is attached to a gas chromatography system.
The eluent exits the GC column (A) and enters the FID detector’s oven (B). The oven is needed to make sure that as soon as the eluent exits the column, it does not come out of the gaseous phase and deposit on the interface between the column and FID. This deposition would result in loss of eluent and errors in detection. As the eluent travels up the FID, it is first mixed with the hydrogen fuel (C) and then with the oxidant (D). The eluent/fuel/oxidant mixture continues to travel up to the nozzle head where a positive bias voltage exists (E). This positive bias helps to repel the reduced carbon ions created by the flame (F) pyrolyzing the eluent. The ions are repelled up toward the collector plates (G) which are connected to a very sensitive ammeter, which detects the ions hitting the plates, then feeds that signal (H) to an amplifier, integrator, and display system. The products of the flame are finally vented out of the detector through the exhaust port (J).
See also[edit]
- Flame detector
- Thermal Conductivity Detector
- Gas Chromatography
- Active fire protection
- Photoionization detector
- Photoelectric flame photometer
References[edit]
- Jump up ^ "Flame Ionisation Detector Principles". www.cambustion.com. Retrieved 3 December 2014.
- Jump up ^ Scott, R. P. W., 1957, Vapour Phase Chromatography, Ed. D. H. Desty (London: Butterworths), p. 131.
- Jump up ^ McWilliam, I. G.; Dewar, R. A. "Flame Ionization Detector for Gas Chromatography". Nature 181 (4611): 760. Bibcode:1958Natur.181..760M. doi:10.1038/181760a0.
- Jump up ^ Morgan, D J (1961). "Construction and operation of a simple flame-ionization detector for gas chromatography". J. Sci. Instrum. 38 (12): 501. Bibcode:1961JScI...38..501M. doi:10.1088/0950-7671/38/12/321. Retrieved 2009-03-18.
- Jump up ^ Harley, J.; Nel, W.; Pretorius, V. (January 18, 1958). "Flame Ionization Detector for Gas Chromatography". Nature. doi:10.1038/1781244b0.
- Jump up ^ "Timeline". Perkinelmer.com. Retrieved 12 Dec 2014.
Sources[edit]
- Skoog, Douglas A., F. James Holler, & Stanley R. Crouch. Principles of Instrumental Analysis. 6th Edition. United States: Thomson Brooks/Cole, 2007.
- Halász, I. & W. Schneider. “Quantitative Gas Chromatographic Analysis of Hydrocarbons with Capillary Column and Flame Ionization Detector.” Analytical Chemistry. 33, 8 (July 1961): 978-982
- G.H. JEFFERY, J.BASSET, J.MENDHAM, R.C.DENNEY, "VOGEL'S TEXTBOOK OF QUANTITATIVE CHEMICAL ANALYSIS."
출처: <http://en.wikipedia.org/wiki/Flame_ionization_detector>
Fast FID Principles
The flame ionisation detector (FID) is the automotive emissions industry standard method of measuring hydrocarbon (HC) concentration.
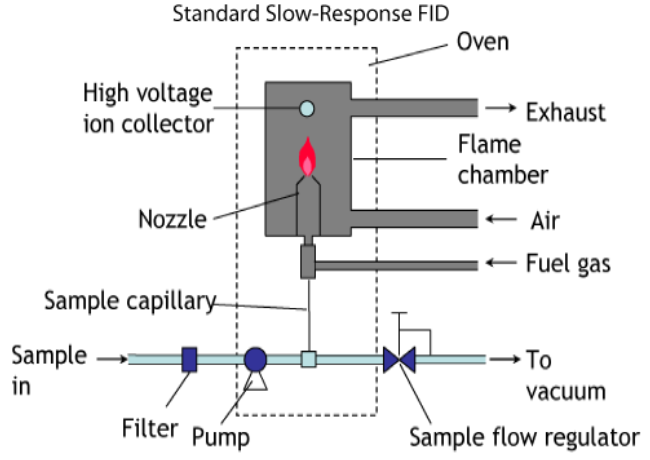
The sample gas is introduced into a hydrogen flame inside the FID. Any hydrocarbons in the sample will produce ions when they are burnt. Ions are detected using a metal collector which is biased with a high DC voltage. The current across this collector is thus proportional to the rate of ionisation which in turn depends upon the concentration of HC in the sample gas.
The ionisation process is very rapid, so the slow time response of conventional FIDs is mainly due to sample handling. A typical slow analyser might have a response time of 1-2 seconds.
The Cambustion HFR fast response FID analyzers use conventional detection principles and a unique patented sampling system to give millisecond response times.
The Cambustion fast FID consists of a main control unit (MCU) and two remote sampling heads (which house the FIDs). The dual channel nature of the instrument enables simultaneous real-time measurement in two locations allowing, for example, evaluation of catalyst performance.
출처: <http://www.cambustion.com/products/hfr500/fast-fid-principles>
GC Solutions #11: The Flame Ionization Detector

by Matthew Klee
In this article we initiate a discussion on the workhorse detector of gas chromatography: the flame ionization detector.
The flame ionization detector (FID) is the premier detector in gas chromatography. It has unique properties and performance that puts it above and beyond all other general-use detectors in gas chromatography (or any other form of chromatography, for that matter).
Topping the list of unique attributes are (1) unit carbon response and (2) wide linear operating range (up to 7 orders of magnitude). When combined with its other attributes of low cost, ease of use, speed of response, and ruggedness, it is no wonder why the FID is the premier detector of choice for GC.
The FID is a mass sensitive detector. That means that its response is proportional to the mass of carbon that passes through it. In that regard, FID response is stated in terms of picograms carbon per sec. Detection limits for FIDs are in the low pg C /sec.
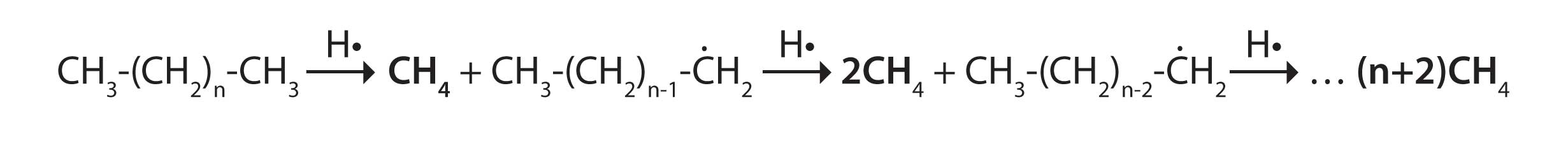
Unit carbon response means that the FID responds linearly to the mass of carbon flowing through it, independent of compound structure. The FID gives unit response for most hydrocarbons within a couple per cent error. Exceptions to this will be discussed next month. This attribute of unit carbon response allows one to quantify mixtures without having calibration standards for every component. Amounts of components in a sample relate to their relative peak areas. So, a simple area per cent report will fairly closely reflect the mass per cent of each component in a mixture. This is extremely useful when analysing complex samples such as those in the petroleum industry wherein samples can contain well over 1000 components. In the same vein, the relative ratio of the area of one peak to another (e.g., the peak of an unknown component relative to a calibrated reference peak) closely reflects its relative amount in the sample. This is useful when estimating concentration levels of components in a sample when identities are unknown or when standards are not available for calibration.
The FID was first described by two independent groups at approximately the same time [1,2]. FIDs were commercially available soon thereafter (the early 1960s.) Most of the developments since the original functional designs have been primarily in areas of usability, adaptation for capillary instead of packed columns, and in improvements of associated electronics, and signal processing.
The Flame
In a hydrogen flame, hydrogen gas (H2) reacts exothermically with the oxygen (O2) to form water. A hydrogen/air flame temperature burns at 2210 °C.*
2H2 + O2 4H• + 2O• 2H2O + heat
In the above reaction, one part oxygen reacts with two parts hydrogen. This ratio (1:2) is called the stoichiometric ratio. Because air is approximately 20% oxygen (O2), a stoichiometric mixture would require an air/hydrogen gas flow ratio of 2:5; 2.5 times more air than hydrogen. Although stoichiometric ratios of oxygen to hydrogen can provide a reasonable dynamic range for the FID, experience has shown (in part because of the complex combustion processes described below) that an excess flow of air is required to ensure complete combustion, unit carbon response and the widest linear dynamic range. In addition, higher than stoichiometric air flow helps to avoid carbon deposits from forming in the jet when high concentrations of analyte or solvent pass through.
A ratio of at least 6:1 of air to hydrogen has empirically been found necessary to achieve the widest dynamic range possible with FID. Many manufacturers recommend ratios of 10:1 or more air/hydrogen flows. The higher the sample load to the FID, the more flame gases are required to prevent blowout and carbon formation. That is why gas flows used with packed columns (higher sample loads) generally need to be higher than when capillary columns are used. Exact flow rates are somewhat instrument specific and also relate a bit to carrier gas flow rates, so following manufacturer recommendations is wise.
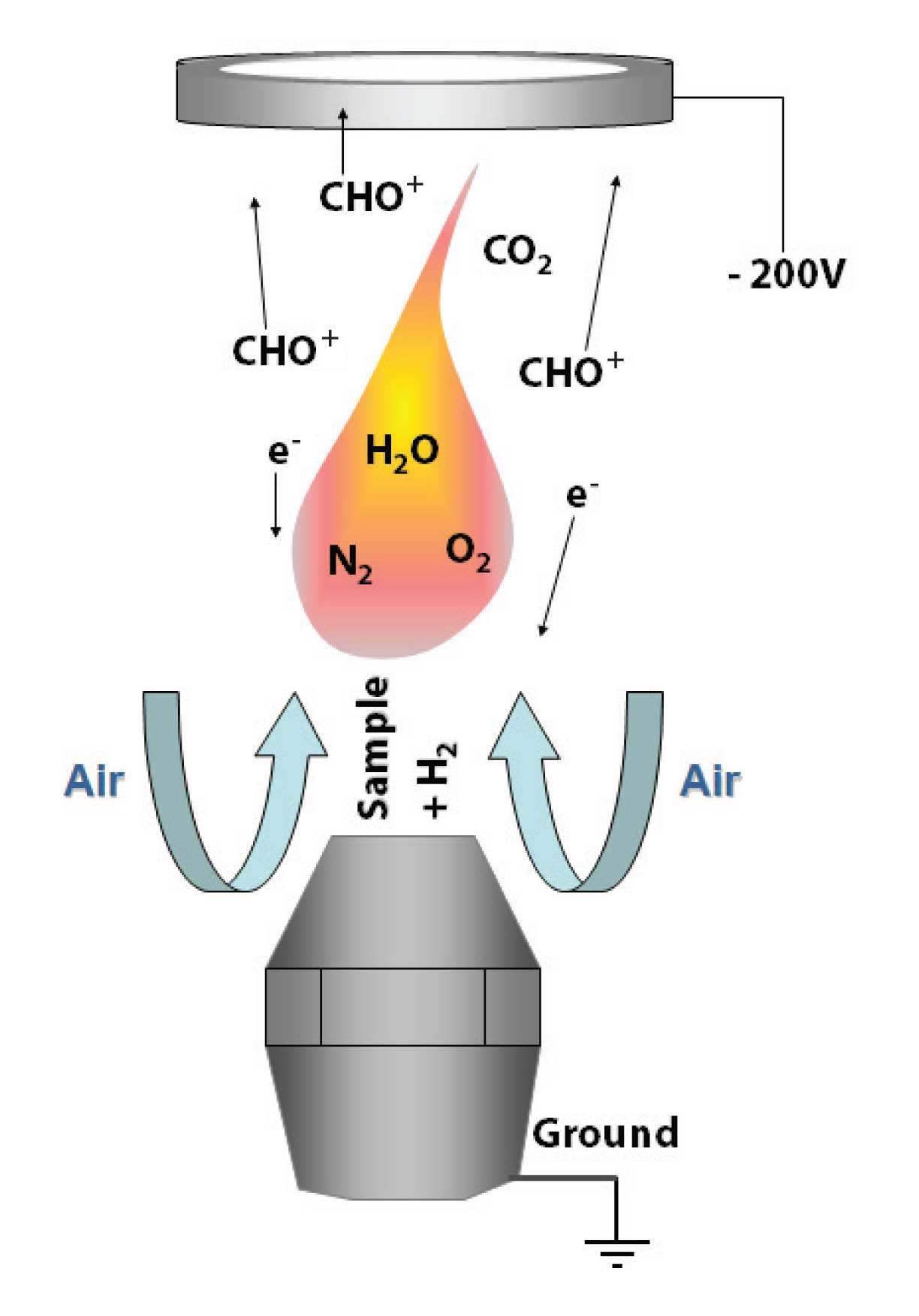
Sample Combustion and Signal Generation
A very nice explanation of FID flame chemistry has been provided by Holm [3]. Therein he supports a mechanism whereby most organic compounds are reduced to saturated counterparts in the initial portion of the flame, where temperatures are lower. As they continue up the flame, these saturated counterparts then continue to react with hydrogen atoms to form methane, as illustrated in Equation 1.
Still further in the flame, methane is combusted to form formylium ion CHO+, the primary FID signal-producing ion.
CH4 → H2 + :CH O•→ CHO* CHO+ + e-
Other reactions can of course occur, including ones that form other positive ions such as hydronium ion.
CHO+ + H2O H3O+ + CO
All positive ions are collected by a negatively biased collector causing a current to flow, which is then electronically amplified and digitized (Figure 1). The current is proportional to the number of ions collected. The yield of ions from carbon passing through the detector is on the order of one ion per 106 carbon atoms [4], yet this is still enough for the FID to give picogram-level detection. Electrons in the flame flow in the opposite direction and are grounded out on the FID jet (Figure 2). By biasing the collector high enough relative to the jet (e.g., -200 V), recombination of positively charged ions and electrons is minimized, and signal maximized.
References
1. J. Harley, W. Nel and V. Pretorious, Nature , London, 181(1958)177.
2. I. G. McWilliams and R. A. Dewer, “Gas Chromatography 1958”, (Ed. D. H.Desty), Butterworths Scientific Publications (1957) 142
3. T. Holm, J. Chrom. A , 842 (1999) 221–227
4. D.K. Bohme, in: P.J. Ausloss (Ed.), Kinetics of Ion–Molecule Reactions, Plenum Press, New York, 1979
Dr Matthew S. Klee is internationally recognized for contributions to the theory and practice of gas chromatography. His experience in chemical, pharmaceutical and instrument companies spans over 30 years. During this time, Dr Klee’s work has focused on elucidation and practical demonstration of the many processes involved with GC analysis, with the ultimate goal of improving the ease of use of GC systems, ruggedness of methods and overall quality of results.
출처: <http://www.sepscience.com/Techniques/GC/Articles/208-/GC-Solutions-11-The-Flame-Ionization-Detector>
PID Control in Melsec
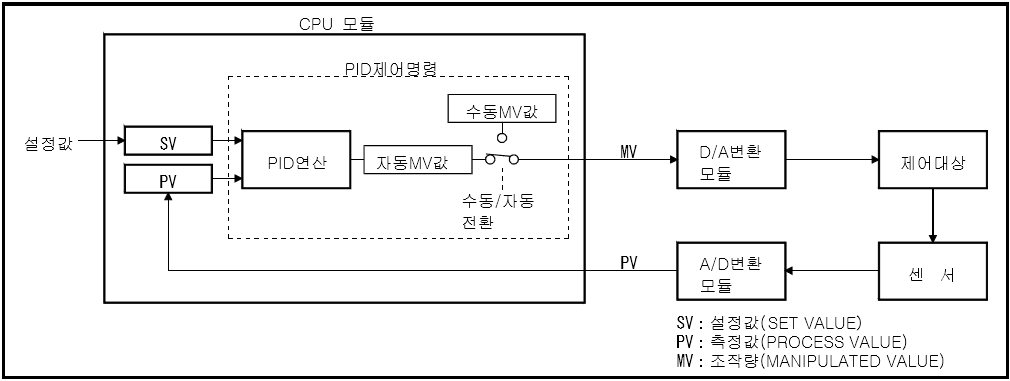
화면 캡처: 2018-11-02 오전 09:54
SV Set Value
PV Process Value
MV Manipulted Value
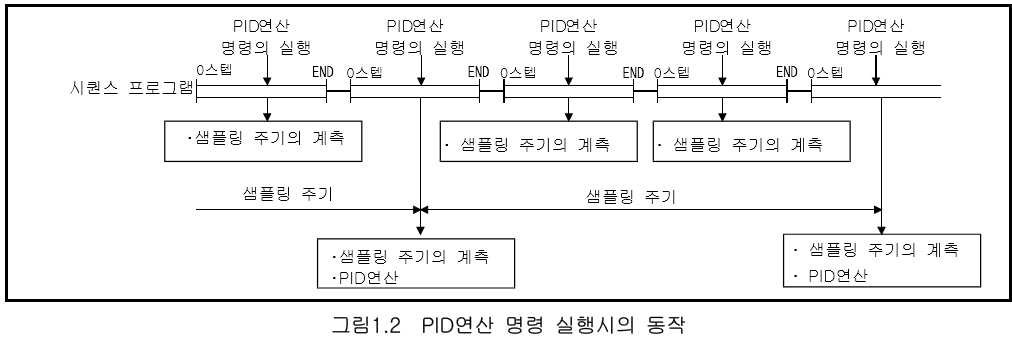
화면 캡처: 2018-11-02 오전 09:55
PID 연산 명령에는
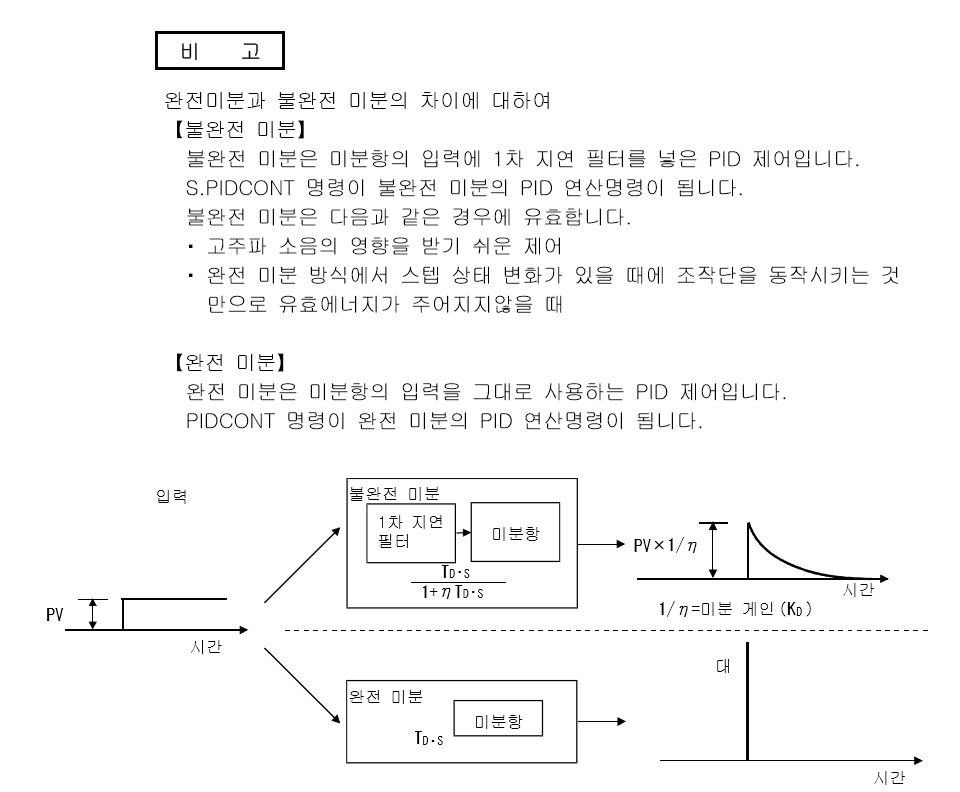
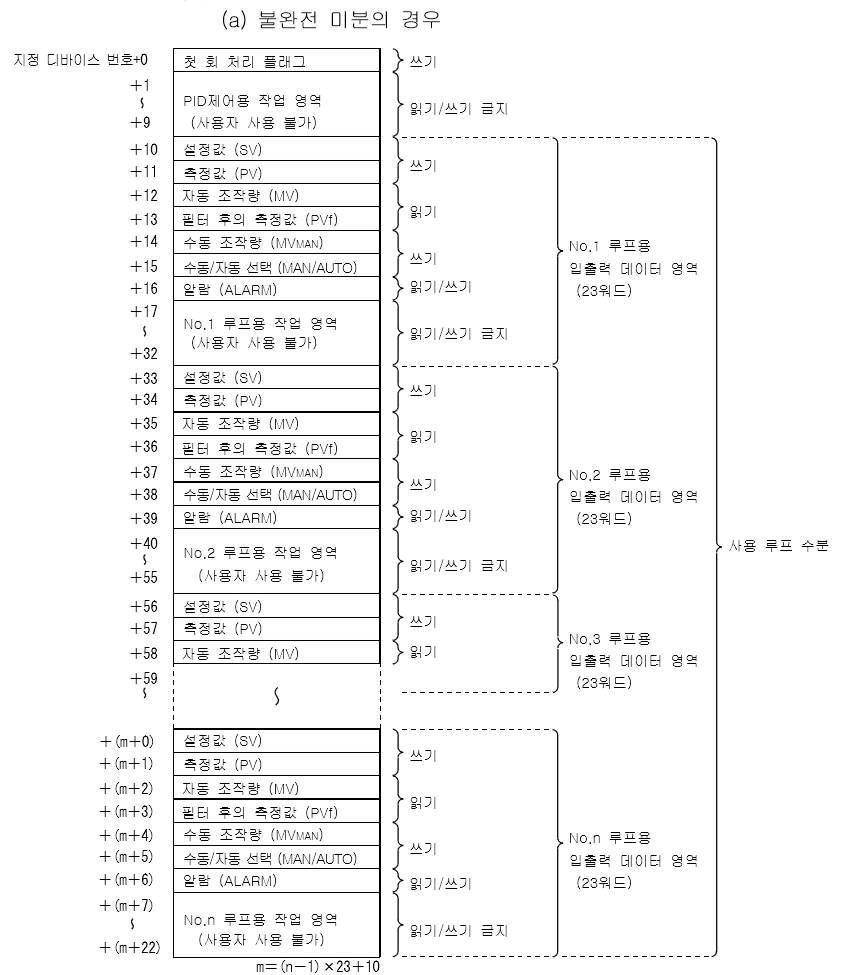
S.PIDCONT 불완전 미분
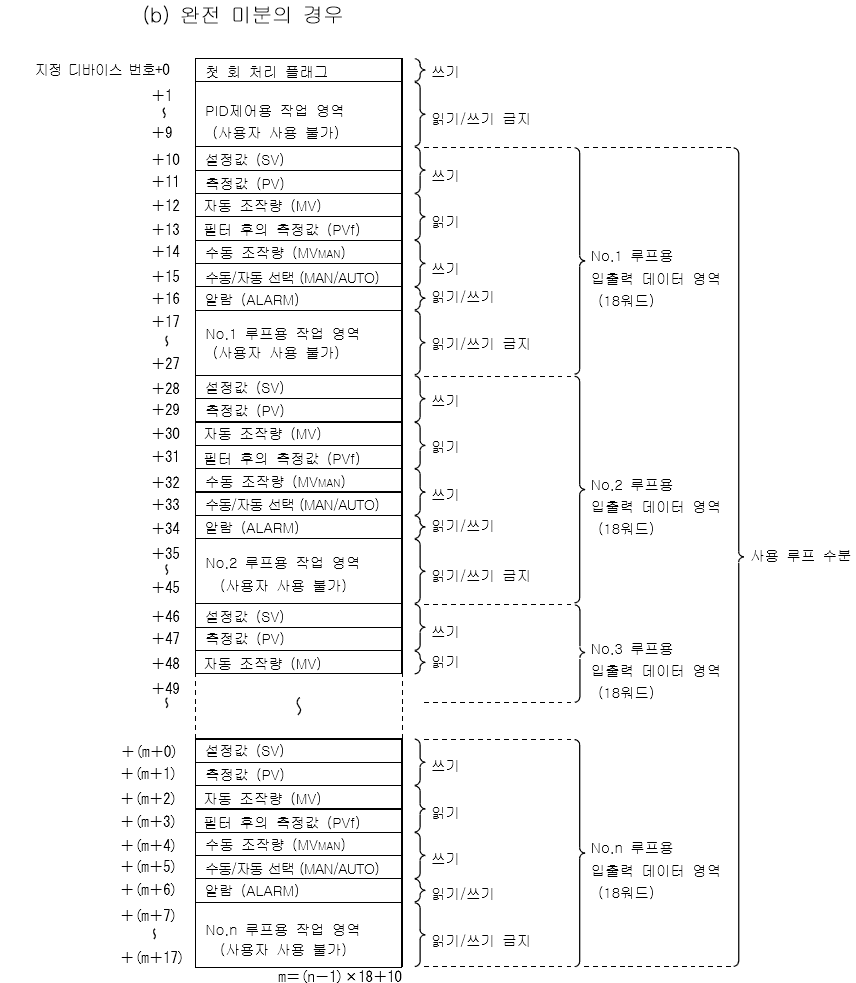
PIDCONT 완전미분
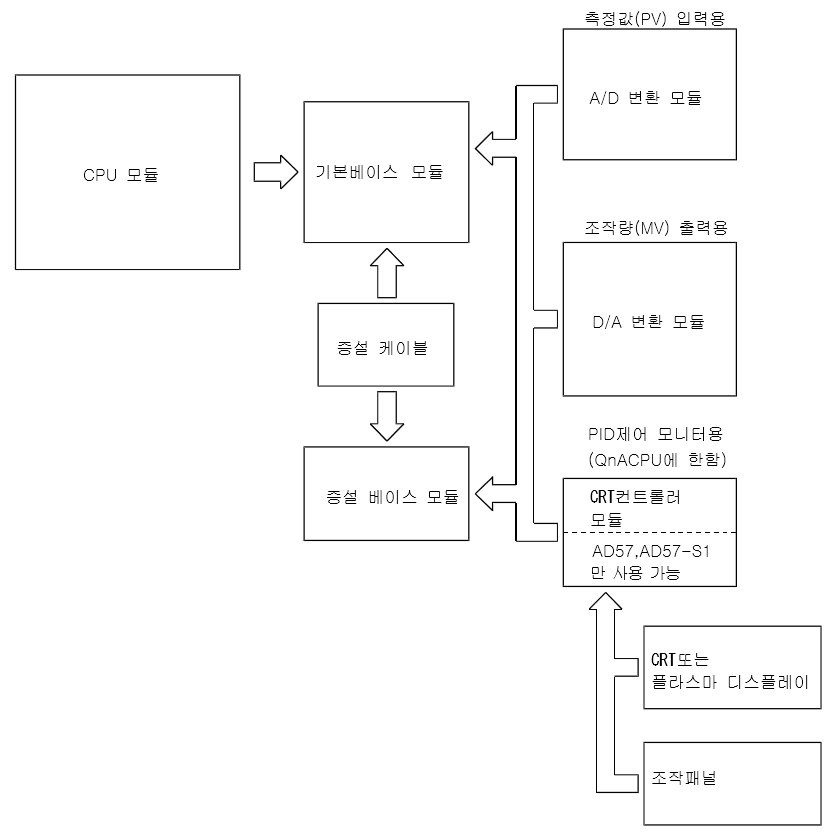
화면 캡처: 2018-11-02 오전 09:57
불완전미분에 대한 성능, 사양
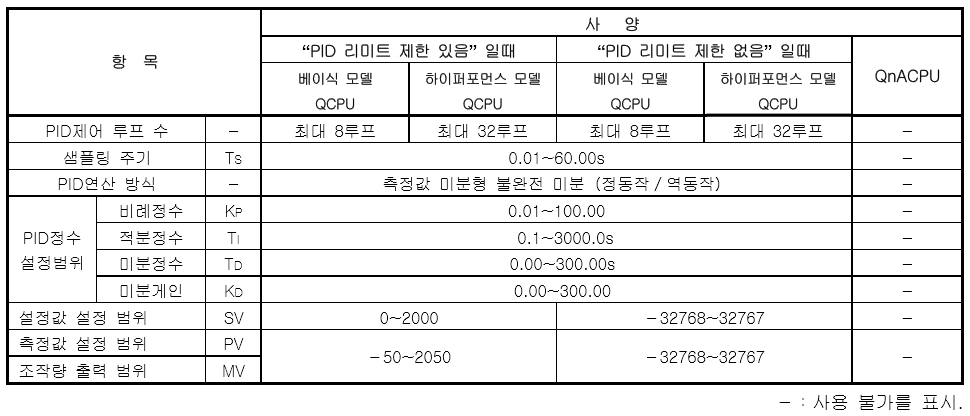
화면 캡처: 2018-11-02 오전 09:58
불완전 미분에 대한 블록도
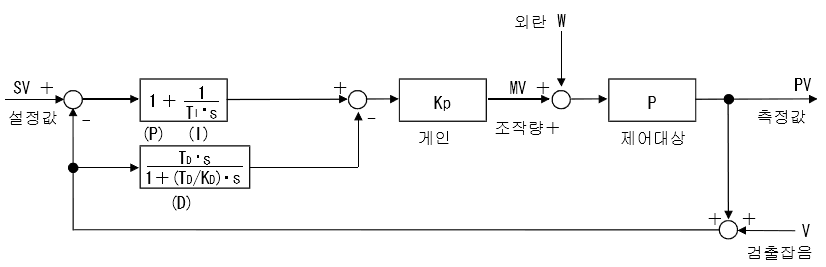
화면 캡처: 2018-11-02 오전 09:59
불완전 미분에 대한 연산식

화면 캡처: 2018-11-02 오전 10:00

화면 캡처: 2018-11-02 오전 10:01
불완전미분에 대한 제어 명령

화면 캡처: 2018-11-02 오전 10:02
완전미분에 의한 PID 제어
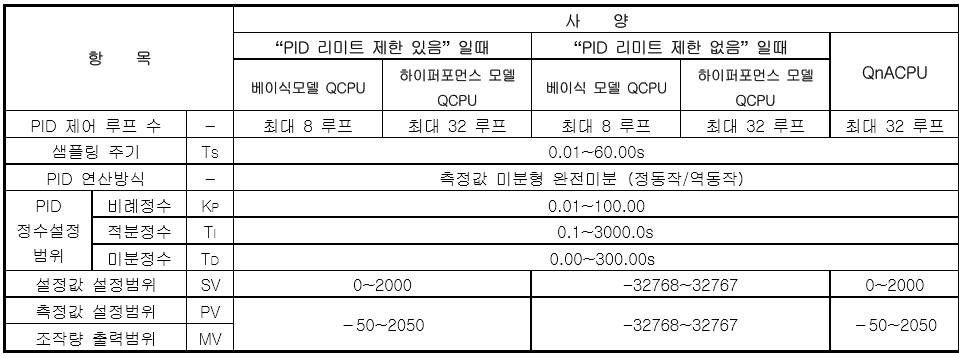
화면 캡처: 2018-11-02 오전 10:06
PID 연산 블록도

화면 캡처: 2018-11-02 오전 10:07

화면 캡처: 2018-11-02 오전 10:07

화면 캡처: 2018-11-02 오전 10:07
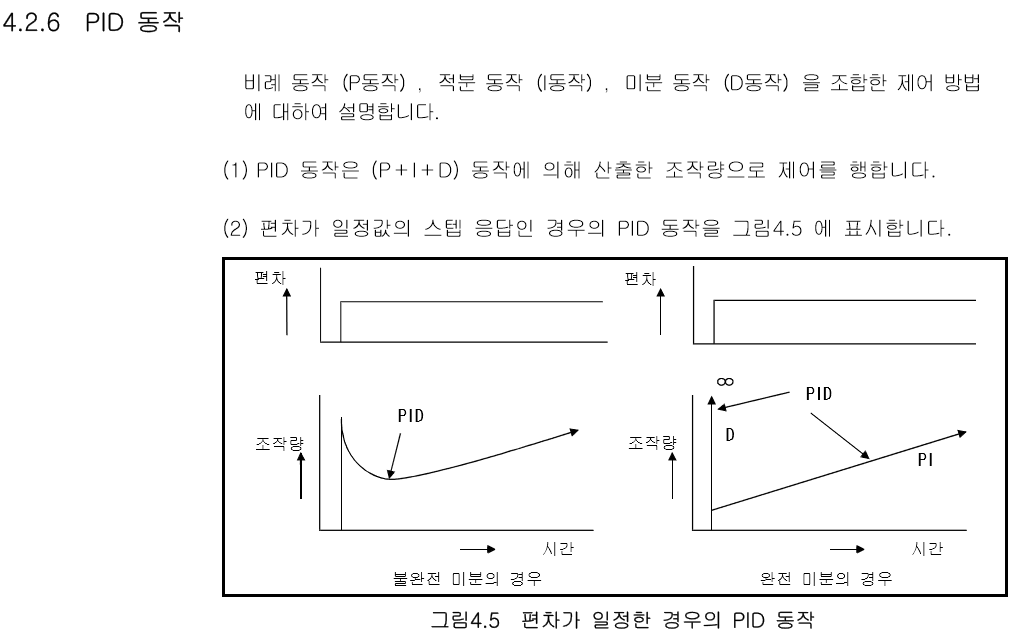
PID 제어 명령
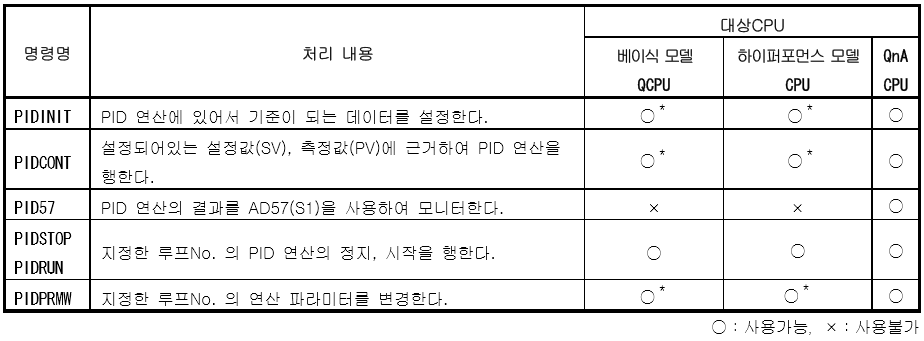
화면 캡처: 2018-11-02 오전 10:08
PID 제어의 기능
2018-11-02 오전 10:10

화면 캡처: 2018-11-02 오전 10:11
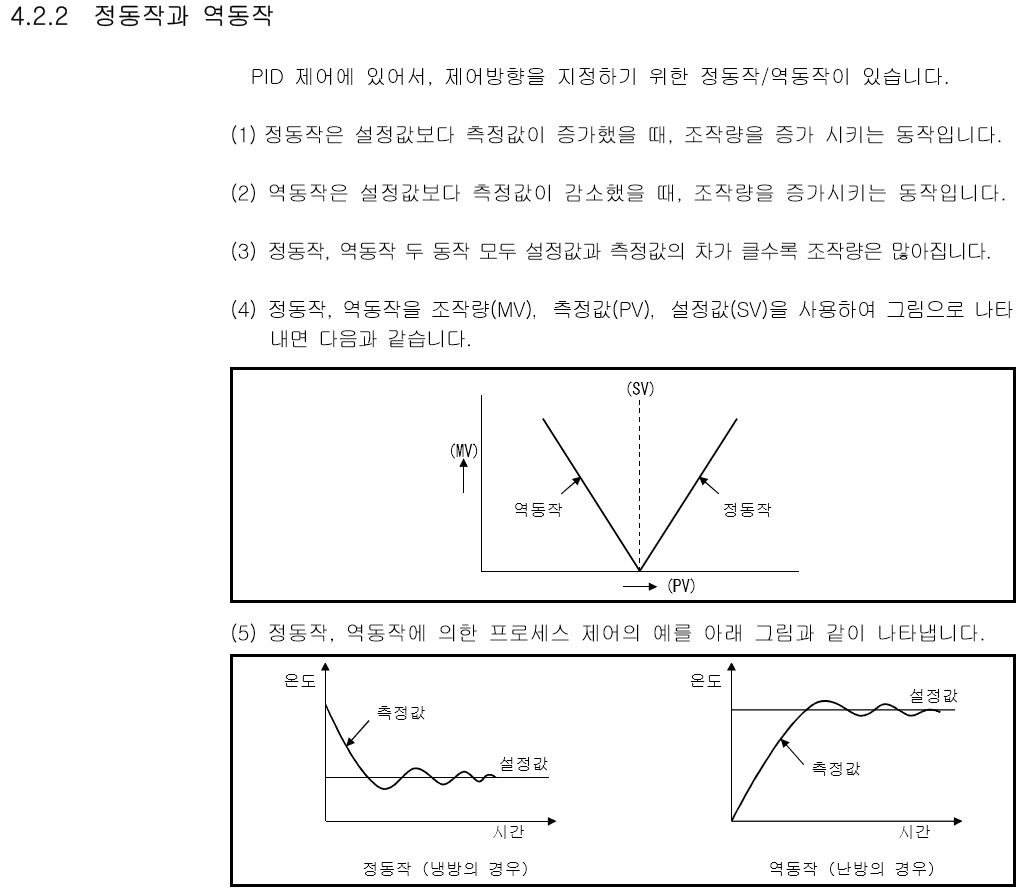
화면 캡처: 2018-11-02 오전 10:11

화면 캡처: 2018-11-02 오전 10:11
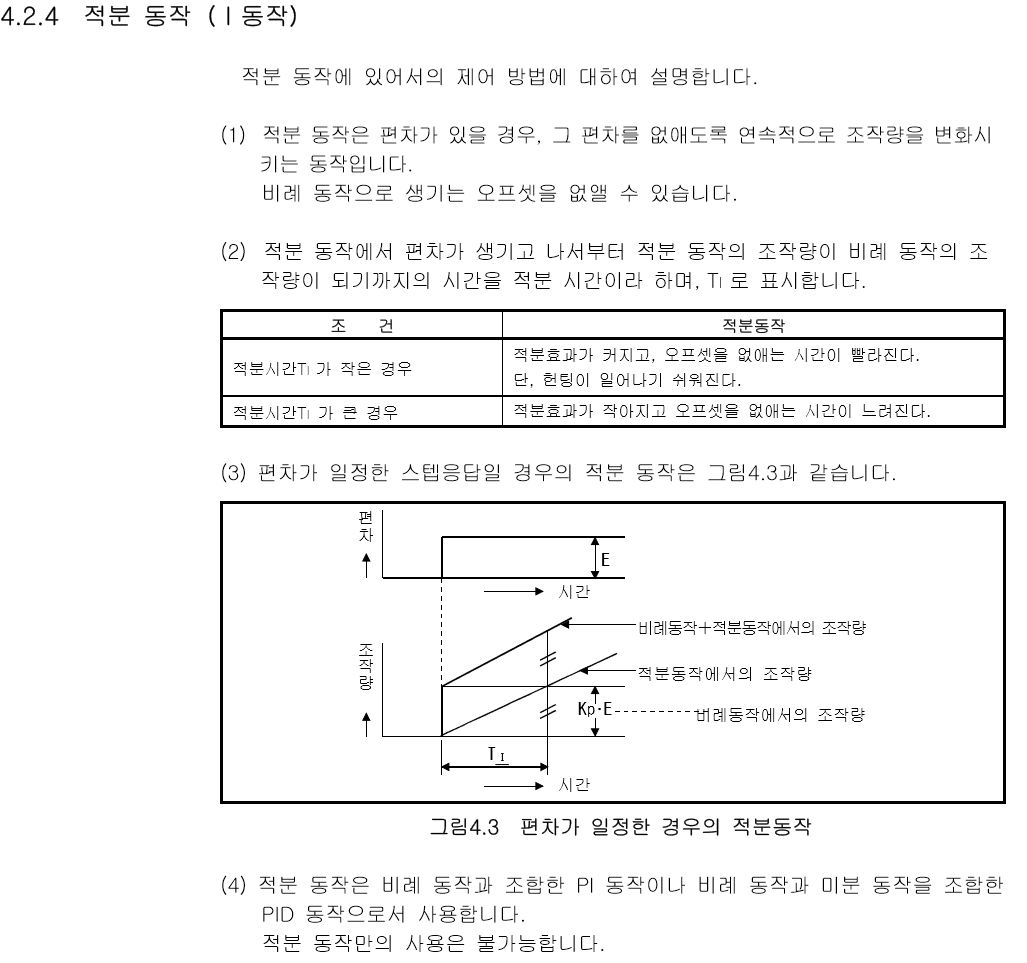
화면 캡처: 2018-11-02 오전 10:12
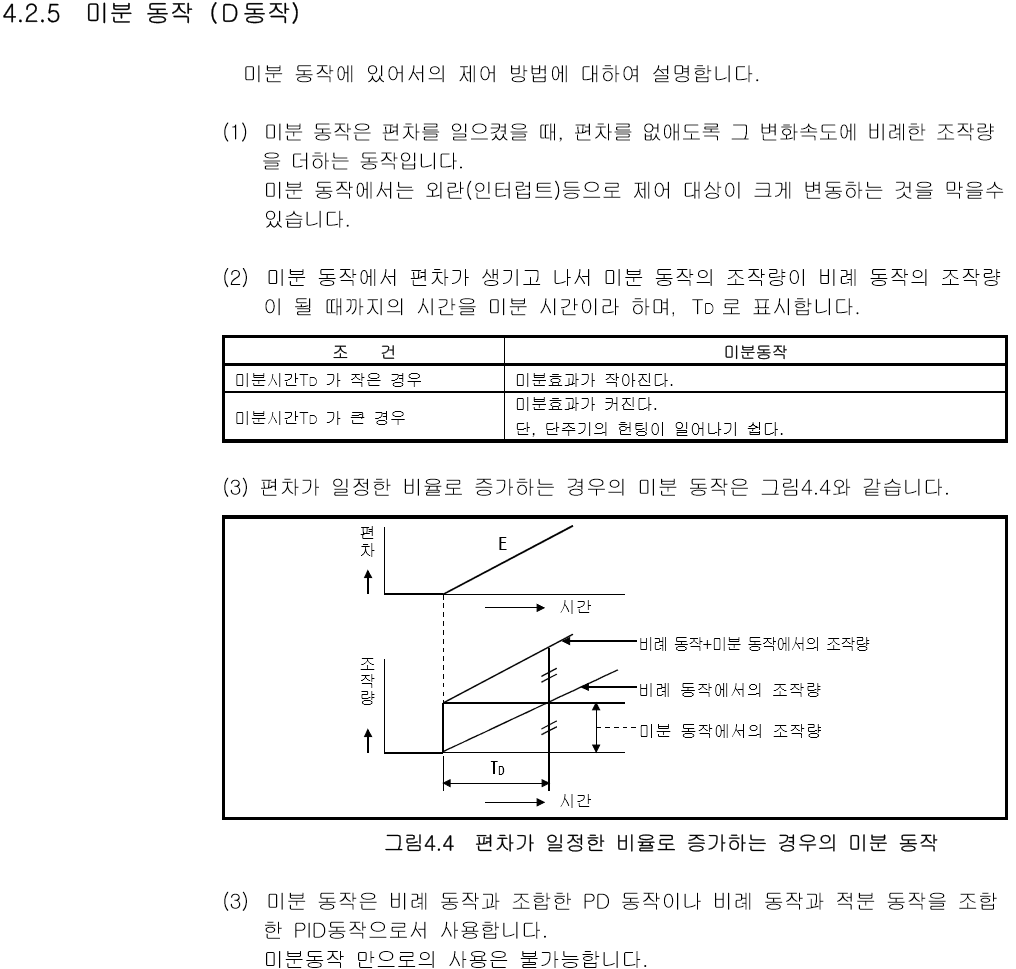
화면 캡처: 2018-11-02 오전 10:15
화면 캡처: 2018-11-02 오전 10:14
화면 캡처: 2018-11-02 오전 10:15

화면 캡처: 2018-11-02 오전 10:16


화면 캡처: 2018-11-02 오전 10:35
화면 캡처: 2018-11-02 오전 10:17

화면 캡처: 2018-11-02 오전 10:42
화면 캡처: 2018-11-02 오전 10:36
화면 캡처: 2018-11-02 오전 10:42
PID Control
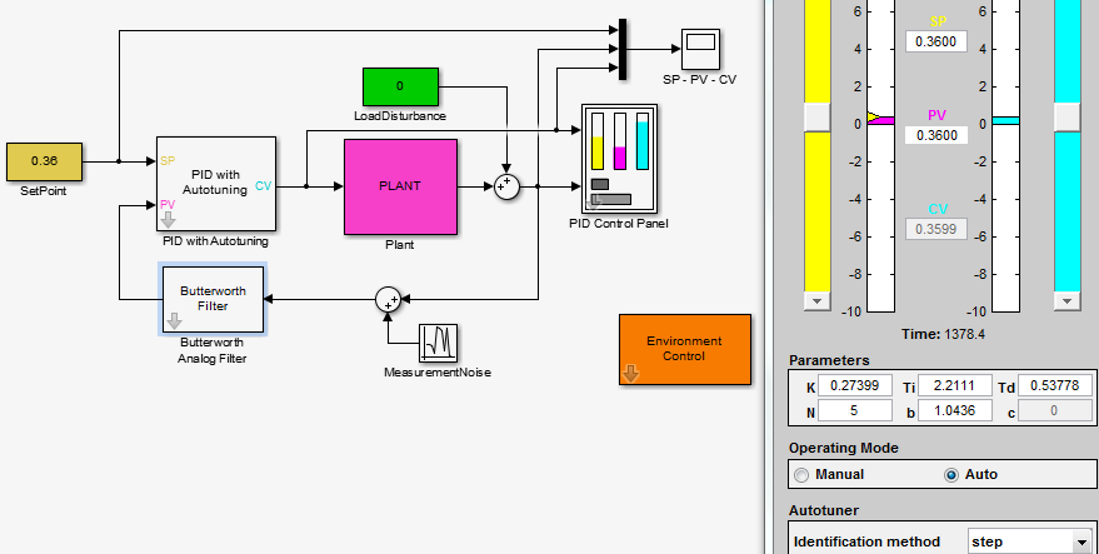
상태 제어가능성 state controllability
출력 제어가능성 output controllability
관측가능성 observability
PID 제어기기의 일반적인 특징은 다음과 같다.
- PID 제어기는 구조가 간단하고 제어 성능이 우수하며, 제어이득 조정이 비교적 쉽기 때문에, 산업현장에서 80%이상을 차지할 정도로 많이 사용되고 있다. PID 제어는 비례제어, 적분제어, 마분제어를 단독으로 사용하거나 혹은 두가지 이상을 결합한 형태로 사용한다.
- 비례(P) 제어는 PID 제어기에서 반드시 사용하는 자장 기본적인 제어이며 구현하기 쉽다. 그러나, 비례제어 만으로는 플렌트에 적분기가 없을 경우에 정상상태 오차가 발생하기 쉽다.
- 적분(I) 제어는 주로 정상상태 오차를 없애기 위해 사용된다. 그러나, 적분 이득을 잘못 조정하면 과도한 오버슈트가 발생하거나 시스템이 불안해 진다.
- 미분(D) 제어는 잘 활용하면 안정성에 기인하고, 예측 기능이 있어 응답속도를 조절 할 수 있다. 하지만 시스템ㅇ 잡음 성분이 있을 때, 미분 값이 커지게 되어 제어 입력에 나쁜 영향을 미치는 단점이 나타난다.
- PID 제어기의 계수들은 근궤적 기법, 주파수 응답기법, 분석적 방법 등을 사용하여 설계할 수 있다.
- PID 제어기에 구동기를 연결하여 사용할 때, 구동기의 포화특성이 있으면 적분누적 integrator windup 현상이 생겨 불안정하게 되는데, 이를 막기 위하여 누적 방지 anti-windup 기법을 사용하여야 한다.
- PID 제어기의 형태는 병렬형이 기본형이지만, 실재로 구현할 때에는 필요에 따라 직렬형으로 하거나 미분기 필터를 부착하는 등 여러가지로 변형되어 쓰인다.
- PID 계수들을 자동적으로 조정하는 것을 auto-tunning 이라 하며, 산업계에서 많이 필요로 하고 있다. 대표적인 방법으로는 Ziegler-Nichols 동조법, Relay 동조법 등이 있으며, 이 방법들은 제어대상 시스템의 모델을 사용하지 않고 간단한 동조 과정을 거쳐 PID 계수를 결정한다.
Melamine
From Wikipedia, the free encyclopedia
Jump to: navigation, search
Not to be confused with Melanin.
This article is about the chemical compound. For the chemically-similar plastic, see melamine resin.
| Melamine | |
| IUPAC name[hide] 1,3,5-Triazine-2,4,6-triamine |
|
| Other names[hide] 2,4,6-Triamino-s-triazine Cyanurotriamide Cyanurotriamine Cyanuramide |
|
| Identifiers | |
| CAS number | 108-78-1 |
| PubChem | 7955 |
| ChemSpider | 7667 |
| UNII | N3GP2YSD88 |
| KEGG | C08737 |
| ChEBI | CHEBI:27915 |
| Jmol-3D images | Image 1 |
| SMILES [show] |
|
| InChI [show] |
|
| Properties | |
| Molecular formula | C3H6N6 |
| Molar mass | 126.12 g/mol |
| Appearance | White solid |
| Density | 1574 kg/m3 |
| Melting point | 345 °C, 618 K, 653 °F (decomposition[1]) |
| Boiling point | Sublimes |
| Solubility in water | 3.240 g/l (20 °C)[1] |
(verify) (what is: / ?) Except where noted otherwise, data are given for materials in their standard state (at 25 °C, 100 kPa) |
|
| Infobox references |
Melamine

i/ˈmɛləmiːn/ is an organic base and a trimer of cyanamide, with a 1,3,5-triazine skeleton. Like cyanamide, it contains 67% nitrogen by mass and, if mixed with resins, has fire retardant properties due to its release of nitrogen gas when burned or charred, and has several other industrial uses. Melamine is also a metabolite of cyromazine, a pesticide. It is formed in the body of mammals who have ingested cyromazine.[2] It has been reported that cyromazine can also be converted to melamine in plants.[3][4]
Melamine combines with cyanuric acid and related compounds to form melamine cyanurate and related crystal structures, which have been implicated as contaminants or biomarkers in Chinese protein adulterations.
Contents
[hide]
- 1 Etymology
- 2 Uses
- 3 Toxicity
- 4 Regulation in food and feed
- 5 Synthesis
- 6 Production in mainland China
- 7 Melamine poisoning by tainted food
- 8 Testing in food
- 9 See also
- 10 References
- 11 External links
[edit] Etymology
The German word melamin was coined by combining the names of 2 other chemical products: Melam (a distillation derivative of ammonium thiocyanate) and Amine.[5][6] Melamine etymology is thus not derived from the root melas (μελας, meaning black in Greek), such as, e.g., the pigment melanin, the hormone melatonin, or the melanotan peptides.
[edit] Uses
Melamine is combined with formaldehyde to produce melamine resin, a very durable thermosetting plastic used in Formica™, melamine dinnerware, laminate flooring and dry erase boards.
Melamine foam is used as insulation, soundproofing material and in polymeric cleaning products, such as Magic Eraser™.
Melamine is one of the major components in Pigment Yellow 150, a colorant in inks and plastics.
Melamine also enters the fabrication of melamine poly-sulfonate used as superplasticizer for making high-resistance concrete. Sulfonated melamine formaldehyde (SMF) is a polymer used as cement admixture to reduce the water content in concrete while increasing the fluidity and the workability of the mix during its handling and pouring. It results in concrete with a lower porosity and a higher mechanical strength, exhibiting an improved resistance to aggressive environments and a longer life-time.
The use of melamine as fertilizer for crops had been envisaged during the '50s and '60s because of its high nitrogen content (2/3).[7] However, melamine is much more expensive to produce than are other common nitrogen fertilizers, such as urea. To be effective as a fertilizer, it is essential that the plant nutrients are released or made available in a manner that matches the needs of the growing crop. The nitrogen mineralization process for melamine is extremely slow, making this product both economically and scientifically impractical for use as a fertilizer.


Melamine dinnerware
Melamine and its salts are used as fire-retardant additives in paints, plastics, and paper.[8]
Melamine derivatives of arsenical drugs are potentially important in the treatment of African trypanosomiasis.[9]
Melamine use as non-protein nitrogen (NPN) for cattle was described in a 1958 patent.[10] In 1978, however, a study concluded that melamine "may not be an acceptable non-protein N source for ruminants" because its hydrolysis in cattle is slower and less complete than other nitrogen sources such as cottonseed meal and urea.[11]
Melamine is sometimes illegally added to food products in order to increase the apparent protein content. Standard tests, such as the Kjeldahl and Dumas tests, estimate protein levels by measuring the nitrogen content, so they can be misled by adding nitrogen-rich compounds such as melamine.There is an instrument (SPRINT) developed by the company CEM Corp that allows the determination of protein content directly in some applications; this cannot be fooled by adding melamine in the sample[12][13]
Melamine is also used as a nitrogen and carbon source for N-doped carbon nanotube. N-CNT's can be prepared via Chemical Vapor Deposition (CVD) method by pyrolysizing melamine under an Ar atmosphere in a horizontal glass tube. A thin film of iron (5 nm) is first deposited on a Si/SiO2 wafer. N-CNT synthesis occurs at a furnace temperatures between 800 - 980oC.[14]
[edit] Toxicity
Melamine is described as being "Harmful if swallowed, inhaled or absorbed through the skin. Chronic exposure may cause cancer or reproductive damage. Eye, skin and respiratory irritant." However, the short-term lethal dose is on a par with common table salt with an LD50 of more than 3 grams per kilogram of bodyweight.[15] U.S. Food and Drug Administration (FDA) scientists explained that when melamine and cyanuric acid are absorbed into the bloodstream, they concentrate and interact in the urine-filled renal microtubules, then crystallize and form large numbers of round, yellow crystals, which in turn block and damage the renal cells that line the tubes, causing the kidneys to malfunction.[16]
The European Union set a standard for acceptable human consumption (Tolerable Daily Intake) of melamine at 0.2 mg per kg of body mass,[17] (previously 0.5 milligrams), Canada declared a limit of 0.35 mg and the US FDA's limit was put at 0.063 mg daily (previously 0.63 mg). The World Health Organization's food safety director estimated that the amount of melamine a person could stand per day without incurring a bigger health risk, the "tolerable daily intake" (TDI), was 0.2 mg per kg of body mass.[18]
[edit] Acute toxicity
Melamine is reported to have an oral LD50 of 3248 mg/kg based on rat data. It is also an irritant when inhaled or in contact with the skin or eyes. The reported dermal LD50 is >1000 mg/kg for rabbits.[19] A study by USSR researchers in the 1980s suggested that melamine cyanurate, commonly used as a fire retardant,[20] could be more toxic than either melamine or cyanuric acid alone.[21] For rats and mice, the reported LD50 for melamine cyanurate was 4.1 g/kg (given inside the stomach) and 3.5 g/kg (via inhalation), compared to 6.0 and 4.3 g/kg for melamine and 7.7 and 3.4 g/kg for cyanuric acid, respectively.
A toxicology study in animals conducted after recalls of contaminated pet food concluded that the combination of melamine and cyanuric acid in diet does lead to acute renal failure in cats.[22] A 2008 study produced similar experimental results in rats and characterized the melamine and cyanuric acid in contaminated pet food from the 2007 outbreak.[23] A 2010 study from Lanzhou University attributed renal failure in humans to uric acid stone accumulation after ingestion of melamine resulting in a rapid aggradation of metabolites such as cyanuric acid diamide (ammeline) and cyanuric acid.[24]
[edit] Chronic toxicity
Ingestion of melamine may lead to reproductive damage, or bladder or kidney stones, which can lead to bladder cancer.[19][25][26][27][28]
A study in 1953 reported that dogs fed 3% melamine for a year had the following changes in their urine: (1) reduced specific gravity, (2) increased output, (3) melamine crystalluria, and (4) protein and occult blood.[29]
A survey commissioned by the American Association of Veterinary Laboratory Diagnosticians suggested that crystals formed in the kidneys when melamine combined with cyanuric acid, "don't dissolve easily. They go away slowly, if at all, so there is the potential for chronic toxicity."[30][31][32]
[edit] Treatment of urolithiasis
Fast diagnosis and treatment of acute obstructive urolithiasis may prevent the development of acute renal failure. Urine alkalinization and stone liberalization have been reported to be the most effective treatments in humans.[24]
[edit] Regulation in food and feed
The United Nations' food standards body, Codex Alimentarius Commission, has set the maximum amount of melamine allowed in powdered infant formula to 1 mg/kg and the amount of the chemical allowed in other foods and animal feed to 2.5 mg/kg. While not legally binding, the levels allow countries to ban importation of products with excessive levels of melamine.[33]
[edit] Synthesis
Melamine was first synthesized by the German chemist Justus von Liebig in 1834. In early production, first calcium cyanamide is converted into dicyandiamide, then heated above its melting temperature to produce melamine. However, today most industrial manufacturers use urea in the following reaction to produce melamine:
6 (NH2)2CO → C3H6N6 + 6 NH3 + 3 CO2
It can be understood as two steps.
First, urea decomposes into cyanic acid and ammonia in an endothermic reaction:
(NH2)2CO → HCNO + NH3
Then, cyanic acid polymerizes to form melamine and carbon dioxide:
6 HCNO → C3H6N6 + 3 CO2
The second reaction is exothermic but the overall process is endothermic.
The above reaction can be carried out by either of two methods: catalyzed gas-phase production or high pressure liquid-phase production. In one method, molten urea is introduced onto a fluidized bed with catalyst for reaction. Hot ammonia gas is also present to fluidize the bed and inhibit deammonization. The effluent then is cooled. Ammonia and carbon dioxide in the off-gas are separated from the melamine-containing slurry. The slurry is further concentrated and crystallized to yield melamine.[34] Major manufacturers and licensors such as Orascom Construction Industries, BASF, and Eurotecnica have developed some proprietary methods.
The off-gas contains large amounts of ammonia. Therefore, melamine production is often integrated into urea production, which uses ammonia as feedstock.
Crystallization and washing of melamine generates a considerable amount of waste water, which is a pollutant if discharged directly into the environment. The waste water may be concentrated into a solid (1.5–5% of the weight) for easier disposal. The solid may contain approximately 70% melamine, 23% oxytriazines (ammeline, ammelide, and cyanuric acid), 0.7% polycondensates (melem, melam, and melon).[35] In the Eurotecnica process, however, there is no solid waste and the contaminants are decomposed to ammonia and carbon dioxide and sent as off gas to the upstream urea plant; accordingly, the waste water can be recycled to the melamine plant itself or used as clean cooling water make-up.[36]
[edit] Production in mainland China
Between the late 1990s and early 2000s, both consumption and production of melamine grew considerably in mainland China. By early 2006, melamine production in mainland China is reported to be in "serious surplus".[37] Between 2002 and 2007, while the global melamine price remained stable, a steep increase in the price of urea (feedstock for melamine) has reduced the profitability of melamine manufacturing. Currently, China is the world's largest exporter of melamine, while its domestic consumption still grows by 10% per year. However, reduced profit has already caused other joint melamine ventures to be postponed there.
Surplus melamine has been an adulterant for feedstock and milk in mainland China for several years now because it can make diluted or poor quality material appear to be higher in protein content by elevating the total nitrogen content detected by some simple protein tests. Actions taken in 2008 by the Government of China has reduced the practice of adulteration, with the goal of eliminating it. Court trials began in December 2008 for six people linked to the scandal and ended in January 2009 with two of the convicts being sentenced to death and executed.[38][39]
[edit] Melamine poisoning by tainted food
Melamine has been involved in several food recalls after the discovery of severe kidney damages of children and pets poisoned by melamine-adulterated food.
[edit] 2007 Animal feed recalls
Further information: 2007 pet food recalls and Chinese protein adulteration
In 2007, a pet food recall was initiated by Menu Foods and other pet food manufacturers who had found their products had been contaminated and caused serious illnesses or deaths in some of the animals that had eaten them.[40][41][42] In March 2007, the US Food and Drug Administration reported finding white granular melamine in the pet food, in samples of white granular wheat gluten imported from a single source in China, Xuzhou Anying Biologic Technology[43] as well as in crystalline form in the kidneys and in urine of affected animals.[44] Further vegetable protein imported from China was later implicated.
In April 2007, The New York Times reported that the addition of "melamine scrap" into fish and livestock feed to give the false appearance of a higher level of protein was an "open secret" in many parts of mainland China, reporting that this melamine scrap was being produced by at least one plant processing coal into melamine.[45] Four days later, the New York Times reported that, despite the widely reported ban on melamine use in vegetable proteins in mainland China, at least some chemical manufacturers continued to report selling it for use in animal feed and in products for human consumption. Li Xiuping, a manager at Henan Xinxiang Huaxing Chemical in Henan Province, stated, "Our chemical products are mostly used for additives, not for animal feed. Melamine is mainly used in the chemical industry, but it can also be used in making cakes."[46] Shandong Mingshui Great Chemical Group, the company reported by the New York Times as producing melamine from coal, produces and sells both urea and melamine but does not list melamine resin as a product.[47]
Another recall incident in 2007 involved melamine which had been purposely added as a binder to fish and livestock feed manufactured in the United States. This was traced to suppliers in Ohio and Colorado.[48]
[edit] 2008 Chinese outbreak
Further information: 2008 Chinese milk scandal
In September 2008, several companies, including Nestlé, were implicated in a scandal involving milk and infant formula which had been adulterated with melamine, leading to kidney stones and other renal failure, especially among young children. By December 2008, nearly 300,000 people had become ill, with more than 50,000 infant hospitalizations and six infant deaths.[49][50][51] In a study published in the New England Journal of Medicine, it was reported that melamine exposure increased the incidence of urinary tract stones by seven times in children.[52] Melamine may have been added to fool government protein content tests after water was added to fraudulently dilute the milk. Because of melamine's high nitrogen content (66% by mass versus approx. 10–12% for typical protein), it can cause the protein content of food to appear higher than the true value.[53][54] Officials estimate that about 20 percent of the dairy companies tested in China sell products tainted with melamine. On January 22, 2009, three of those involved in the scandal (including one conditional sentence) were sentenced to death in a Chinese court.[55]
In October 2008, "Select Fresh Brown Eggs" imported to Hong Kong from the Hanwei Group in Dalian in northeastern China, were found to be contaminated with nearly twice the legal limit of melamine. York Chow, the health secretary of Hong Kong, said he thought animal feeds might be the source of the contamination and announced that the Hong Kong Centre for Food Safety would henceforward be testing all mainland Chinese pork, farmed fish, animal feed, chicken meat, eggs, and offal products for melamine.[56]
As of July 2010, Chinese authorities were still reporting some seizures of melamine-contaminated dairy product in some provinces, though it was unclear whether these new contaminations constituted wholly new adulterations or were the result of illegal reuse of material from the 2008 adulterations.[57][58]
On characterization and treatment of urinary stones in affected infants, the New England Journal of Medicine printed an editorial in March 2009, along with reports on cases from Beijing, Hong Kong and Taipei.[59]
Urinary calculi specimens were collected from 15 cases treated in Beijing and were analyzed as unknown objects for their components at Beijing Institute of Microchemistry using infrared spectroscopy, nuclear magnetic resonance, and high performance liquid chromatography. The result of the analysis showed that the calculus was composed of melamine and uric acid, and the molecular ratio of uric acid to melamine was around 2:1.[60]
In a 2009 study of 683 children diagnosed in Beijing in 2008 with nephrolithiasis and 6,498 children without nephrolithiasis aged < 3 years, investigators found that in children exposed to melamine levels < 0.2 mg/kg per day, the risk for nephrolithiasis was 1.7 times higher than in those without melamine exposure, suggesting that the risk of melamine-induced nephrolithiasis in young children starts at a lower intake level than the levels recommended by the World Health Organization.[61]
In a study published in 2010, researchers from Beijing University studying ultrasound images of infants who fell ill in the 2008 contamination found that while most children in a rural Chinese area recovered, 12 per cent still showed kidney abnormalities six months later. "The potential for long-term complications after exposure to melamine remains a serious concern," the report said. "Our results suggest a need for further follow-up of affected children to evaluate the possible long-term impact on health, including renal function."[62] Another 2010 followup study from Lanzhou University attributed the uric acid stone accumulation after ingestion of melamine to a rapid aggradation of metabolites such as cyanuric acid diamide (ammeline) and cyanuric acid and reported that urine alkalinization and stone liberalization were the most effective treatments.[24]
[edit] Testing in food
Until the 2007 pet food recalls, melamine had not routinely been monitored in food, except in the context of plastic safety or insecticide residue. This could be due to the previously assumed low toxicity of melamine, and the relatively expensive methods of detection.
Following the 2008 deaths of children in China from powdered milk, the Joint Research Centre (JRC) of the European Commission in Belgium set-up a website about methods to detect melamine.[63] In May 2009, the JRC published the results of a study that benchmarked the ability of labs around the world to accurately measure melamine in food. The study concluded that the majority of labs can effectively detect melamine in food.[64]
In October 2008, the U.S. Food and Drug Administration (FDA) issued new methods for the analysis of melamine and cyanuric acid in infant formulations in the Laboratory Information Bulletin No 4421.[65] Similar recommendations have been issued by other authorities, like the Japanese Ministry of Health, Labor and Welfare,[66] both based on liquid chromatography – mass spectrometry (LC/MS) detection after hydrophilic interaction liquid chromatography (HILIC) separation.[67]
The existing methods for melamine determination using a triple quadrupole liquid chromatography – mass spectrometry (LC/MS) after solid phase extraction (SPE) are often complex and time consuming. However, electrospray ionization methods coupled with mass spectrometry allow a rapid and direct analysis of samples with complex matrices: the native liquid samples are directly ionized under ambient conditions in their original solution. In December 2008, two new fast and inexpensive methods for detecting melamine in liquids have been published on-line in the Chem. Comm. Journal of the Royal Society of Chemistry (UK).[68]
Ultrasound-assisted extractive electrospray ionization mass spectrometry (EESI-MS) has been developed at ETH Zurich (Switzerland) by Zhu et al., (2008)[69][70] for a rapid detection of melamine in untreated food samples. Ultrasounds are used to nebulize the melamine-containing liquids into a fine spray. The spray is then ionised by extractive electrospray ionisation (EESI) and analysed using tandem mass spectrometry (MS/MS). An analysis requires 30 seconds per sample. The limit of detection of melamine is a few nanograms of melamine per gram of milk.[citation needed]
Huang et al., (2008)[71][72] have also developed at Purdue University (US) a simpler instrumentation and a faster method by using a low-temperature plasma probe to ionize the samples. The major obstacles being solved, the ESI-MS technique allows now high-throughput analysis of melamine traces in complex mixtures.
The Melaminometer[73][74] was a hypothetical design for a synthetic biology circuit, to used for detecting melamine and related chemical analogues such as cyanuric acid. The conceptual project is hosted at OpenWetWare as open source biology in collaboration with DIYbio and has been discussed in various newspapers in the context of homebrew biotechnology. As of October 2009, the design has not been verified.
Because melamine resin is often used in food packaging and tableware, melamine at ppm level (1 part per million) in food and beverage has been reported due to migration from melamine-containing resins.[75] Small amounts of melamine have also been reported in foodstuff as a metabolite product of cyromazine, an insecticide used on animals and crops.[76]
The Food Safety and Inspection Service (FSIS) of the United States Department of Agriculture (USDA) provides a test method for analyzing cyromazine and melamine in animal tissues.[77][78] In 2007, the FDA began using a high performance liquid chromatography test to determine the melamine, ammeline, ammelide, and cyanuric acid contamination in food.[79] Another procedure is based on surface-enhanced Raman spectroscopy (SERS).[80][81]
Member States of the European Union are required under Commission Decision 2008/757/EC[82] to ensure that all composite products containing at least 15% of milk product, originating from China, are systematically tested before import into the Community and that all such products which are shown to contain melamine in excess of 2.5 mg/kg are immediately destroyed.
출처: <http://en.wikipedia.org/wiki/Melamine>
기후변화의 자연적인 원인


7만 4천 년 전에 분화한 인도네시아의 토바 화산은 현재 세계 최대의 칼데라호인 토바 호수가 되어 있다. <출처: (cc) Edubucher at Wikimedia.org>
초창기의 인류는 전 세계로 퍼져나가던 중 7만 4천 년 전에 멸절의 위기를 한 차례 맞았었다. '초화산(supervolcano)'인 토바 화산이 분화를 했기 때문이다. 빙심 시추와 해양퇴적물에 의해 토바 화산의 실체가 드러났다.
이 화산의 폭발이 일어나고 수십 년 동안의 얼음 코어 속 산소동위원소 비율은 지난 수만 년을 통틀어 가장 낮았다. 다시 말해 토바 화산이 폭발한 뒤 수십 년 동안은 빙하기가 최고조에 달했을 때보다도 더 추웠다는 것이다. 지구 전역에 걸쳐 기온이 16℃ 정도 하강한 것으로 추정된다. 적도에서 멀리 떨어진 지역일수록 기온이 더 많이 떨어졌다.
이처럼 기후조건이 악화되면서 식량이 줄어들고 전염병이 창궐했다. 인류는 기근과 질병이라는 두 가지 재앙 앞에 무기력했다. 유럽과 중국 북부에 살던 초기 인류는 아마 완전히 멸종했을 것이다. 기후변화의 영향이 가장 적게 미쳤던 지역의 인류만이 살아남을 수 있었다. 그곳이 바로 아프리카였다. 이전의 인류가 멸절되고 아프리카에서 현생 인류가 퍼져 나온 것은 바로 토바 화산 때문이었다.
1. 태양 복사량의 변화
1941년에 세르비아의 천문학자 밀란코비치(Milutin Milanković, 1879~1958)는 과거 100만 년 동안의 지구궤도 운동에 대해 연구했다. 그는 이 연구로 지구에 도달하는 태양 복사량을 밝힌 정밀한 계산 결과를 발표했다.

기후역사의 연구에 엄청난 기여를 한 세르비아의 천문학자 밀란코비치.
밀란코비치가 이 계산을 했던 북반구의 고위도 지방은 기후변화를 파악함에 있어 중요한 지역이다. 빙하기를 이루기 위해 필요한 거대한 대륙 빙상이 형성되고 소멸되는 지역이기 때문이다. 밀란코비치는 여름 동안 태양 복사에너지가 줄어든 기간을 분석했다.
그는 이 데이터와 65만 년에 걸쳐 유럽 대륙 전역에서 일어났다고 알려진 네 번의 빙하기 사이에 긴밀한 상관관계가 있다는 것을 발견했다. 밀란코비치 이전에도 지구의 기후변동이 천문학적 요인 때문이라고 주장한 학자들은 있었다. 그러나 밀란코비치처럼 정확하게 분석한 과학자는 없었다.
태양 복사에너지의 차이는 여러 가지 원인에 의해 발생한다. 궤도변화는 지구에 도달하는 태양 복사량에 영향을 준다. 따라서 지구의 장기적인 기후변화에 중대한 요인으로 작용한다. 지구에 도달하는 태양 복사량에 변화를 일으키는 궤도변화는 3가지가 있다. 지구궤도의 형태와 연관된 이심률, 지축의 기울기인 경사도의 변화, 세차운동 등이다.
이심률(eccentricity)
이심률은 지구궤도의 형태 변화를 나타낸다. 태양 주위를 공전하는 지구의 궤도는 완전한 원이 아니다. 지구의 공전궤도는 오랜 기간에 걸쳐 원에 가까운 형태에서 타원형으로 점차 변하다가 다시 원형으로 되돌아간다.
지구가 태양에서 가장 멀리 있을 때와 가장 가까이 있을 때 태양 복사에너지의 차이는 이심률 차이의 4배보다 조금 더 크다. 지구궤도는 원에서 타원으로 움직이며 매 9만 6천 년마다 다시 돌아온다. 시간이 지남에 따라 타원의 장축 길이가 변화하는 것이다.
이심률이 0인 원형 궤도 |
이심률이 0.5인 궤도 |
지구와 태양이 가장 가까운 위치(1억 4,600만㎞)에 있는 지점을 근일점, 지구와 태양이 가장 먼 거리에 위치한 지점을 원일점이라 한다. 이심률의 변화는 전체 연간 태양 복사열의 약 0.3%의 차이를 가져온다. 그러나 이 정도로도 계절변화를 만들 수 있다. 만약 지구의 공전궤도가 완벽한 원이었다면 태양에너지의 계절변화는 없었을 것이다.
경사도의 변화(obliquity)

경사도의 변화
경사도의 변화는 지구의 공전궤도면(지구궤도가 만들어내는 가상의 면)에 대한 지축의 기울기 변화와 연관이 있다. 밀란코비치는 오랜 시간 수작업으로 지축의 경사 감소가 여름철 복사량의 감소를 가져온다는 사실을 밝혀냈다. 그리고 그 효과가 위도에 따라 다르다는 것도 밝혀냈다.
고위도의 지구-태양 거리 경사주기는 4만 1,000년, 적도의 주기는 2만 2,000년이었다. 그는 기후의 영향을 받는 적설이 여름철 복사의 변화에 따라 얼마나 증가할 수 있는지를 알아냈다. 산악의 설선(snow lines) 자료를 사용한 그의 분석은 정확한 것으로 후에 밝혀졌다.
지축이 기울어져 있기 때문에 지구에는 계절이 나타난다. 아울러 계절에 따른 태양 복사에너지의 진폭이 생긴다. 지축의 기울기는 최소 21.5도에서 최대 24.5도 사이를 오르락내리락한다. 현재의 기울기는 23.5도에 가깝고 점점 줄어들고 있다. 서기 1만 년경에는 최솟값에 도달할 것으로 예측된다.
세차운동(axial precession)
세 번째 궤도 메커니즘은 세차운동이라고 하는 춘분점(북반구의 경우) 이동과 연관된 근일점 경도의 변화다. 간단히 말해서 시간의 흐름에 따른 지축의 요동을 말한다. 태양계의 다른 행성, 주로 목성과 토성이 지구에 미치는 인력에 의해 나타난다.

세차운동
세차운동으로 인해 항성을 기준으로 한 지구 자전축의 회전 방향이 바뀐다. 따라서 세차운동은 1년 중 지구의 공전궤도가 태양에 가장 가까운 지점인 근일점과 가장 먼 지점인 원일점이 나타나는 시기를 변화시킨다. 약 1만 9,000년과 2만 3,000년의 주기를 가지고 있다.
세차운동은 (위도 0°인 적도에 미치는 경사의 영향과는 다르게) 열대지방에 가장 중요한 영향을 미친다. 열대지방에 발생하는 일사량의 직접적인 효과는 세차운동에 의해 조절된 이심률 때문이다.
현재는 보다 정교한 기후이론이 나오고 있지만 밀란코비치의 발견은 기후역사의 연구에 엄청난 기여를 했다. 20세기 후반기의 기후학 연구는 대부분 지구 대기의 서로 다른 기후 되먹임 과정(climate-feedbackmechanism)을 밝히고 평가하는 것과 연관이 있었다. 밀란코비치의 연구는 이 되먹임 과정의 내용을 정확하게 예측했다. 그가 세심하게 계산한 궤도 이론은 지난 200만 년 동안 빙하기가 발생한 원인을 설명할 수 있었던 것이다.
2. 태양 흑점의 변화
기원후 지구 역사상 가장 추웠던 시기가 17세기 중반이었다. 어떤 원인으로 그토록 추웠던 것일까? 천문학자들의 연구에 의하면 당시에 태양의 흑점이 거의 발생하지 않았다고 한다. 즉 소빙하기 중에서도 가장 추웠던 17세기 중반은 태양의 표면에 생기는 흑점의 수가 현저히 감소한 시대와 정확히 일치한다.
그렇다면 지구의 기후변화에 태양 흑점이 영향을 준 것일까? 많은 학자들이 연구에 연구를 거듭했다. 태양 흑점은 기원전에 중국의 천문학자들이 발견한 바 있다. 동양의 기록을 분석해보면 태양 흑점의 증감을 알 수 있다.
갈릴레이는 망원경을 이용해 태양 흑점을 관측한 후 상세한 기록을 남겼다. 그 기록에 따르면 서기 1645년에서 1715년까지는 태양 흑점이 거의 관측되지 않았다. 이 시기를 태양 흑점의 극소기라 하여, 기후와 태양 흑점변화의 연관성을 입증한 영국의 천문학자 에드워드 마운더(Edward Walter Maunder, 1851~1928)의 이름을 따 '마운더 극소기'라고 부른다.

태양 흑점 개수의 변화 <출처: NASA>
흑점현상이 많아지면 태양에는 주위보다 온도가 높은 백반(白班)현상이 증가한다. 태양표면이 활발하게 대류운동을 한다는 뜻으로 폭발이나 플레어(flare)1) 현상도 자주 발생한다. 따라서 태양의 복사에너지는 흑점이 많을 때 크고, 적을 때는 작아진다. 그래서 흑점을 소빙하기의 원인으로 꼽았고 태양 흑점의 변화를 연구해 기후변화를 추정하는 것이다.
그러나 최근 탐측기술이 발달하면서 흑점 수 변화에 따른 입사에너지의 변동이 1㎡ 당 약 1~2와트로 매우 작다는 사실이 밝혀졌다. 최근 기후학자들은 태양의 흑점활동이 소빙하기의 한랭한 기후를 만들었다고 보지 않는다. 다만 흑점현상으로 인한 자외선 복사감소의 2차적 영향, 우주선(cosmic rays) 강도의 변동 등 여러 가능성이 겹쳐졌을 것으로 보고 있다.
3. 지각운동과 화산분출
지구가 처음부터 지금의 대륙과 해양의 모습을 하고 있었던 것은 아니다. 계속적인 지각운동으로 변화를 거듭해 왔다. 판구조론에서 설명하는 것 처럼 지각운동의 영향으로 대륙의 위치와 크기가 바뀌었다. 해양분지의 형태나 배열에도 커다란 변화가 있었고, 산지와 고원의 크기와 위치도 변화되어 왔다. 그 결과 세계적인 대기대순환(大氣大循環)과 해양순환의 패턴이 바뀌게 되었다.
해양순환이 바뀌면 표층해류나 심층해류가 바뀐다. 또 대륙 위치의 변화는 주요 빙하기(페름·석탄기의 빙하기)뿐 아니라 습윤하거나 건조한 환경이 발달한 시기(페름·트라이아스)가 나타나도록 했다. 현재 티베트 고원과 히말라야 산맥이 융기하고 있는 것도 지각운동의 하나다. 이로 인해 중국 서부와 중앙아시아 지역으로 건조한 사막 환경이 발달하게 된 것이다.
짧은 시간에 가장 많은 기후변화를 가져오는 것 중의 하나가 화산 분출이다. 강력한 폭발성 화산 분화는 먼지와 이산화황 분진을 성층권으로 분출시킨다. 이로 인해 지구 상공에 화산 분진이 돌면서 극심한 기후변화가 일어난다. 적도에서 분화된 물질들은 양쪽 반구로 확산된다. 그러나 중위도에서 분출되어 고위도로 확산되는 것은 분출된 반구 쪽으로만 영향을 준다.

파푸아뉴기니 타부르부르 화산의 분화 <출처: (cc) Taro Taylor at Wikimedia.org>
화산의 분화 기록들은 남극과 그린란드 빙상에 보존되어 있다. 최근에 가장 큰 영향을 준 화산 분화는 1815년의 탐보라 화산2) 분화이다. 다량의 화산 물질이 성층권으로 치솟으면서 북반구에 3년 동안 여름이 없는 기후를 만들었다. 이로 인해 식량감산과 유럽의 폭동, 발진티푸스, 장티푸스의 창궐, 금융대공황이 발생했다.
4. 대기 조성의 변화
온실효과가 반드시 인간이 배출하는 이산화탄소의 증가만으로 일어나는 것은 아니다. 인간의 산업활동과 구별되는, 대기 조성의 변화로 발생하는 자연적인 온실효과도 상당하다. 예를 들어 열염대순환의 변화로 인한 해양에서의 미량 기체의 흡수가 있다. 또 지표 식생에 미치는 빙기-간빙기 변화는 대기 중 이산화탄소와 메탄 함량의 변화를 가져온다.
온실가스(이산화탄소나 메탄)와 지구 온도의 변화는 빙기와 간빙기 동안에 실제로 동시에 일어났다. 그렇기에 명확한 원인을 알기는 어렵다. 많은 기후학자들은 극 빙상 연구로 나타난 대기 중 이산화탄소의 장기간 및 단기간의 변화 모두가 해양과 육지의 생물 활동과 해양 해류 순환이 복합적으로 작용한 것으로 보고 있다.
이 외에 기후를 변화시킬 가능성이 있는 자연적인 원인으로 혜성이나 소행성 또는 큰 운석들과의 충돌이 있다. 지구는 지난 수십억 년 동안 외계물질과의 수없는 충돌에 의해 지금의 질량을 갖게 된 것이다.

캐나다의 퀘벡 주에 있는 운석 구덩이
대표적인 사례가 멕시코 유카탄 반도에 떨어진 거대한 운석이다. 이 운석의 직경은 5~15㎞ 정도로 추정된다. 운석이 지구에 부딪치면서 엄청난 지각변동과 함께 먼지가 성층권까지 솟아올랐다. 결국 대량의 먼지가 성층권과 대류권 내의 에어러졸3)을 증가시켰고 이것이 지구의 기후를 바꾼 원인이 되었다. 에어로졸이 태양빛을 가리면서 기온이 뚝 떨어진 것이다. 당시 지구에 번성했던 공룡 등의 파충류들은 변온동물이라 추운 날씨를 견디지 못하고 멸종한 것으로 보인다.
글
반기성 | 케이웨더 기후산업연구소장
연세대 천문기상학과 및 대학원 졸업하고, 공군 기상전대장과 한국기상학회 부회장을 역임했다. 현재 케이웨더 기후산업연구소장이며, 조선대학교 대기과학과 겸임교수로 있다. 연세대에도 출강하고 있다. 저서로는 [워렌버핏이 날씨시장으로 온 까닭은?], [날씨가 바꾼 서프라이징 세계사] 등 15권이 있다.
'지구별 이야기 > 기후와 지구온난화' 카테고리의 다른 글
| 북극진동 (1) | 2016.12.15 |
|---|---|
| Stabilizing Climate (1) | 2016.12.12 |
| Is the Supermoon responsible for record low Polar ice formation? (0) | 2016.11.22 |
| Lowest amount of sea ice ever seen by humans during... (0) | 2016.11.22 |
| 올 겨울 춥다는데 (0) | 2016.11.18 |
공포의 런던 스모그
[기후재난 현장을 가다] 공포의 런던 스모그…맑은 하늘 되찾기 수십년 걸렸다
A14면1단| 기사입력 2016-12-13 20:33 | 최종수정 2016-12-13 21:21
1952년 극심한 스모그 런던 덮쳐 / 사고 빈발… 응급실에 환자 넘쳐나 / 5일간 4000여명 주민 사망하기도 / 1956년 대기청정법 만들며 개선 / 미세먼지·아황산가스 밀도 급감 / 오염원 변화 발맞춰 규제 확대도
"네, 이게 런던이에요. 걱정하지 말아요. 런던이 이렇게 안개에 숨어있는 날은 겨울철 며칠뿐이에요." 체코의 유명 일러스트레이터 미로슬라프 샤셰크가 2004년 발간한 동화책 '이것이 런던입니다(This is London)'의 첫 페이지는 황갈색으로 메워진 채 시작한다. 안개가 자욱하게 낀 스모그의 도시 런던을 형상화한 것이다. 지난달 영국 남부 항구도시 브라이턴에서 만난 존 베넷(56)씨는 샤셰크의 책 첫 장을 보여주며 어린 시절 봤던 런던을 회상했다. 그의 아버지는 1950년대까지 런던에서 거주하다 60년대 브라이턴으로 이주했다. 새로운 일자리를 찾기 위해서이기도 했지만, 런던의 공기가 참을 수 없이 혼탁해진 것도 그가 이주하게 된 이유 중 하나였다. 베넷씨는 "아버지를 따라 어릴 적 런던에 간 적이 몇 번 있었는데, 그 당시 런던에서 쾌청한 날씨를 만나기란 매우 어려웠다"며 "젊은 세대들이 예전보다 맑아진 공기를 누리고 있어 다행"이라고 말했다. 영국에는 베넷씨 가족과 같은 경험이 있는 사람들을 쉽게 찾을 수 있다. 영국의 젊은 세대들도 할아버지·할머니 세대에 일어난 '런던스모그' 이야기를 듣고 자랐다.
런던 하늘의 어제와 오늘 1952년 12월 스모그로 시야가 확보되지 않는 런던 거리에서 교통정리 담당자가 손전등을 들고 버스가 갈 길을 밝히고 있다(왼쪽). 런던 시민들이 지난달 7일 중심가인 스트랜드 거리를 활보하고 있다. 런던=정선형 기자·영국기상학회 제공 |
런던스모그는 1952년 12월4∼8일 런던지역에 이어진 극심한 스모그다. 런던의 가정과 인근 공장에서 내뿜은 매연과 이산화황가스 등이 겨울철 차가운 공기와 합쳐져 도시에 내려앉아 정체되면서 나타난 현상이었다. 당시 런던의 평균 시계는 3∼5㎞였지만 런던스모그 사태가 발생한 5일 동안은 짙은 안개로 버스와 열차 교통사고가 빈발했다. 악화된 대기질로 응급실에는 심장발작이나 호흡곤란을 호소하는 환자들로 넘쳐났다. 영국 보건환경국은 5일간의 스모그로 당시 4000여명의 주민이 사망했다고 밝혔다.
1952년 12월 스모그로 시야가 확보되지 않는 런던 스트랜드 거리에서 런던 경찰이 버스가 갈 길을 밝히기 위해 불을 들고 서 있다. 영국기상학회 제공 |
◆60년 전 이뤄진 '대기오염방지법'… 과실을 얻은 후손들
런던스모그가 일어난 지 65년의 시간이 흐른 지금 런던의 대기질은 크게 개선됐다. 런던 중심에 위치한 트래펄가 광장과 광장에서 이어진 스트랜드 거리는 지난달 방문 당시 매우 쾌청한 상태를 보이고 있었다. 미세먼지 농도도 23㎍/㎥에 불과해 국내 기준으로 '좋음' 수준을 보였다.
이런 변화의 중심에는 영국 정부가 1956년 만든 '대기청정법'(Clean Air Act)이 자리하고 있다. 올해로 60주년을 맞은 이 법은 공장, 기차 등 공공시설에서부터 일반 가정에서 때는 석탄연료까지 규제하는 내용을 담고 있다. 지방자치단체에서는 매연감독관(Smoke Inspector)을 임명해 과도한 매연을 내뿜은 공장이나 가정을 규제해 벌금을 물리기도 했다.
1952년 12월 스모그로 시야가 확보되지 않는 런던 거리에서 교통정리담당자가 손전등을 들고 버스가 갈 길을 밝히고 있다. 영국기상학회 제공 |

영국 정부는 이에 그치지 않고 주된 환경오염 원인의 변화에 발맞춰 법을 순차적으로 개정하고 적용 대상을 확장해 나갔다. 1968년 법 적용 대상을 확장한 데 이어 1993년에는 미세먼지, 탄화수소, 다이옥신 등 새로운 오염물질도 규제대상에 포함했다.
영국 정부는 대기청정법에서 나아가 2020년에는 대기오염이 심각한 5개 도시에 '대기청정구역'(Clean Air Zone)을 설치할 예정이다. 5개 도시는 리즈 버밍햄 노팅엄 더비 사우샘프턴이다. 이 지역에서는 오염물질을 많이 배출하는 노후 버스 등 교통수단을 운행할 수 없다. 개인 차량은 제외된다.
런던 시민들이 지난달 7일 중심가인 스트랜드 거리를 활보하고 있다. 런던=정선형 기자 |
이 같은 노력에 의해 오늘날의 런던을 비롯한 영국의 잉글랜드 지역은 연평균 미세먼지 분포도가 세계보건기구(WHO) 권장기준인 10㎍/㎥에 가까운 수준으로 개선됐다. 법이 만들어진 60년 전에 비해 런던의 대기중 아황산가스 밀도는 300분의 1수준으로 낮아졌다.
영국은 여기서 그치지 않고 대기청정법 60주년을 맞아 왕립외과협회(Royal College ofPhysician)를 중심으로 '실내 대기오염'에 대한 연구에도 박차를 가하고 있다. 연구를 맞은 스티븐 홀게이트 RCP 석좌교수는 "대기청정법을 만든 후 60년간 대기오염이 인체에 미치는 영향을 추적연구했다"고 밝히며 "대기오염은 체내에 축적되는 방식이라 한번 오염물질을 흡입하면 이 물질이 지속적으로 건강에 영향을 미친다"고 말했다. 또 기술 발달에 따라 대기오염의 방식이 달라지고 있어 그 시대에 맞는 오염방지 방안을 만드는 게 중요하다고 조언했다.

◆더 나은 공기를 위해… 정부 상대 소송전도 벌여
이런 노력에도 영국 시민들은 정부가 대기질 개선에 더 많은 노력을 쏟아붓길 기대하고 있다. 최근에는 과거 대기오염에 따른 만성질환으로 사망한 런던 시민이 수천명에 달한다는 연구 결과도 발표돼, 이에 대해 정부가 책임져야 한다는 주장도 제기되고 있다.
런던 해크니 지역에 위치한 공익법률시민단체 '클라이언트어스'(ClientEarth)는 3년 전 정부를 상대로 낸 소송에서 승소한 뒤 올해부터 2차 소송을 진행하고 있다. 1차 소송에서 패소한 정부가 법원이 제시한 개선안에 따라 대기오염을 줄여나가야 했지만, 이를 이행하지 못해 2차 소송을 진행하고 있다는 게 이들의 설명이다. 지난달 사무소에서 만난 클라이언트어스의 활동가 안드리아 리(43·여)는 "정부가 독일 자동차 회사 폴크스바겐이 연비를 조작한 사건이 불거져 이 때문에 개선안을 이행하지 못했다고 주장하고 있다"며 "깨끗한 공기를 위해 계속 정부를 법률로써 압박하는 것도 하나의 방안"이라고 설명했다.
영국 학계에서는 관련 연구도 계속되고 있다. RCP의 홀게이트 교수는 "대기오염을 방지하는 방법은 단순히 오염물질을 규제하는 데 그치지 않고, 일반 시민들의 체력 증진도 함께 고려해야 한다"며 런던에서 일고 있는 자전거 타기 운동을 소개하기도 했다. 의사이기도 한 그는 "자동차를 타고 다니면서 살이 쪘다고 불평하기보다 걷고, 자전거를 타면서 환경을 지키는 방법을 생각해야 합니다"고 덧붙였다.
1953년 11월 도시노동자들이 오염된 공기를 걸러내기 위한 마스크를 쓰고 거리를 걷고 있다. 가디언 제공 |
◆ "대기오염 한 번 노출돼도 만성질환 겪어"
"한번 대기오염에 노출되면 이는 그 사람의 평생에 영향을 미칩니다. 공기가 맑은 곳으로 이주해도 소용이 없죠."
지난달 영국 런던 왕립외과협회(Royal College of Physician)에서 만난 스티븐 홀게이트(Stephen Holgate·아래 사진) 석좌교수는 지난 2월 자신이 발표한 논문 '매일 우리가 쉬는 숨: 대기오염의 생애주기 영향(Every breath we take: the lifelong impact of airpolution)'을 보여주며 이같이 말했다.
홀게이트 교수는 영국 정부의 '대기청정법'이 시작된 지 60주년을 맞는 올해를 위해 2년여간 이번 논문을 준비했다. 60년 전 런던스모그를 비롯한 오염된 공기 속에서 살던 사람들과 반대로 깨끗한 환경에서 살던 사람들을 추적조사했다. 그 결과 한번 대기오염으로 피해를 본 신체는 깨끗한 공기가 있는 지역에 가더라도 쉽게 나아지지 않는 만성적 질환을 겪게 된다는 결론을 얻었다.
이런 연구 결과 때문에 홀게이트 교수는 "대기오염 방지 방안을 좀 더 실생활에 밀접한 분야를 통해 해결할 필요가 있다"고 주장했다. 이와 함께 그는 외부의 대기오염에 비해 실내 대기오염의 심각성이 크게 부각되지 않는 점을 염려했다.
그는 대기오염 문제를 해결하기 위해 △장기적 대책 수립 △전문가와 일반인에 대한 교육 강화 △차량용 친환경 대체연료 개발 △오염발생자에 책임부과 △대기환경 감시시스템 도입 △대기오염 악화 시 시민보호 대책 마련 △불공평 해소 △노약자 보호 등 총 14가지 권고사항을 논문을 통해 밝혔다.

그는 대기오염이 3단계로 나뉜다고 설명했다. 1단계는 '공장굴뚝'으로 대표되는 산업혁명에 따른 대기오염, 2단계는 '자동차 배기구'로 상징되는 자동차 수 증가에 따른 대기오염이다. 최근 3단계인 '실내 대기오염'이 새로운 연구과제로 떠올랐다. 홀게이트 교수는 "헤어스프레이는 물론, 음식을 할 때 나오는 탄소가스 등도 건강을 해치는 요인 중 하나"라고 했다. 그는 "사실 자동차 배기가스만 하더라도 바로 앞의 차량에서 뒤에 차량으로 들어오는 무색 무취의 공기가 가장 위험하다. 하지만 사람들은 이런 위험성을 간과하고 있다"며 밀폐된 공간에서의 대기오염에도 주목해야 하는 이유를 설명했다.
1980년대 초를 시작으로 한국을 수차례 방문한 그는 "한국의 전통가옥이 실내 대기오염을 방지하는 데 가장 적합한 구조를 띠고 있다"며 "각각 분리된 공간을 두고 있는 데다가 문을 열면 환기하기 좋은 구조이기 때문에 이상적"이라고 설명했다.
런던=글·사진 정선형 기자 linear@segye.com
ⓒ 세상을 보는 눈, 글로벌 미디어 세계일보
북극진동
'북극진동' 교란…20년 새 최악 한파 예고
A14면1단| 기사입력 2016-12-13 22:10
ㆍ북극 기온 기록적으로 높아 찬바람 묶는 제트기류 붕괴
ㆍ동북아·북미 강추위 '비상'

북극의 찬 소용돌이 바람이 올겨울 중위도 지역을 덮칠 것으로 보인다. 미국 언론들은 이르면 15일(현지시간)부터 이례적인 한파가 닥치고, 중서부 지역 기온이 20년 새 최저 기록을 경신할 것이라고 보도했다. 찬 바람을 북극권에 묶어두던 제트기류가 약해지면서 찬 바람이 북미와 러시아 시베리아, 동북아시아와 북유럽을 덮칠 것으로 예상된다.
지난 11일부터 미국 아이오와, 일리노이, 인디애나 등 몇몇 주에서는 20㎝ 넘는 눈이 쌓였다. NBC 등은 미 중서부 주들과 캐나다 국경에 걸쳐진 5대호 일대에 강추위가 예상된다고 보도했다. 오하이오의 경우 평년 기온보다 25도나 낮다. 캐나다 언론들도 올겨울 이례적인 한파를 예보했다. 미국에서는 2014년 1월 북극 찬 바람이 밀려내려와 한파가 몰아닥쳤다. 기상학자들은 당시와 지금의 기상 상황이 비슷하며, 중위도 지역의 평균기온이 20년 새 최저치로 떨어질 수도 있다고 경고했다.
중위도 지역의 이례적인 한파는 북극진동이 교란됐기 때문이다. 북극진동은 북극의 찬 소용돌이 바람이 강약을 되풀이하는 현상을 말한다. 북극진동 자체는 이상 현상이 아니다. 지구가 열대지방에서 남아도는 열을 북극으로 옮기려는 에너지 순환작용의 일부다. 문제는 찬 바람을 가둬두는 제트기류가 기후변화로 붕괴하면서 북극진동의 패턴이 달라지고 북극의 찬 바람이 더 남쪽으로 내려오게 되는 것이다.
북극의 찬 공기는 고기압이고 중위도의 따뜻한 공기는 저기압이어서 극지방을 감싸는 제트기류가 생긴다. 그런데 북극이 따뜻해져 중위도 지역과의 온도 차이가 줄어들면 제트기류가 약해진다. 지난달 북극 평균기온이 평년보다 20도나 올라가는 등 올해 북극은 기록적으로 높은 기온을 보이고 있다. 몇몇 지역에서는 더운 바람이 밀고 올라가고 또 다른 지역에서는 찬 바람이 남쪽으로 내려오는데, 현재는 북극진동이 2개로 조각나다시피 했다. 밀려내려온 북극권의 찬 공기 중 한 덩어리는 러시아 쪽, 한 덩어리는 북미 대륙을 덮고 있다. 기상학자들은 올겨울 북극의 찬 바람이 더 자주, 더 남쪽으로 내려올 것이며 고위도와 중위도의 접경선인 북미와 동북아시아 일대가 영향권에 들어갈 것으로 봤다.
<박효재 기자 mann616@kyunghyang.com>
©경향신문(www.khan.co.kr), 무단전재 및 재배포 금지
'지구별 이야기 > 기후와 지구온난화' 카테고리의 다른 글
| 기후변화의 자연적인 원인 (0) | 2016.12.15 |
|---|---|
| Stabilizing Climate (1) | 2016.12.12 |
| Is the Supermoon responsible for record low Polar ice formation? (0) | 2016.11.22 |
| Lowest amount of sea ice ever seen by humans during... (0) | 2016.11.22 |
| 올 겨울 춥다는데 (0) | 2016.11.18 |

'관련기술' 카테고리의 다른 글
| TGA, 열중량분석기 (0) | 2016.12.12 |
|---|---|
| 열분석결과의 해석, TGA, DSC (0) | 2016.12.12 |
| VOC 제거를 위한 환경촉매 설계 (0) | 2016.11.11 |
| 촉매연소 기술을 이용한 대기오염 저감 기술 (0) | 2016.11.11 |
| 활성탄소 섬유 (0) | 2016.10.27 |
TGA, 열중량분석기

'관련기술' 카테고리의 다른 글
| DSC, TGA (0) | 2016.12.12 |
|---|---|
| 열분석결과의 해석, TGA, DSC (0) | 2016.12.12 |
| VOC 제거를 위한 환경촉매 설계 (0) | 2016.11.11 |
| 촉매연소 기술을 이용한 대기오염 저감 기술 (0) | 2016.11.11 |
| 활성탄소 섬유 (0) | 2016.10.27 |









































